题目内容
17.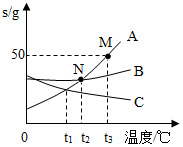 如图所示曲线A,B,C分别表示三种固体物质的溶解度变化,试回答:
如图所示曲线A,B,C分别表示三种固体物质的溶解度变化,试回答:(1)t2℃,A,B,C三种物质的溶解度大小关系是A=B>C:
(2)M点表示t3℃时,A的饱和(饱和、不饱和)溶液,t3℃把30gA物质加入到50g水中,得到溶液质量为75克.
(3)当B中混有少量A时,可采用蒸发结晶的方法提纯B.
(4)若要将C物质接近饱和的溶液变成饱和,可采用改变温度的方法为升温
(5)t1℃,A,B,C三种物质的饱和溶液升温到t3,溶液溶质质量分数由大到小关系是B>A>C.
分析 (1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)溶解度曲线上的点表示该温度下物质的饱和溶液,并据该温度下A的溶解度分析解答;
(3)据AB的溶解度受温度影响情况分析提纯物质的方法;
(4)C的溶解度随温度升高而减小,故要将其不饱和溶液变为饱和溶液可采取升温的方法;
(5)据物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数分析解答.
解答 解:(1)t2℃,A,B,C三种物质的溶解度大小关系是:A=B>C;
(2)M点表示t3℃时,A的饱和溶液,t3℃时A的溶解度是50g,即100g水中最多溶解50g的A,所以把30gA物质加入到50g水中,最多溶解25g,得到溶液质量为 75克;
(3)A的溶解度受温度影响较大,B的溶解度受温度影响较小,所以当B中混有少量A时,可采用 蒸发结晶的方法提纯B;
(4)C的溶解度随温度升高而减小,故要将其不饱和溶液变为饱和溶液可采取升温的方法;
(5)t1℃,A,B,C三种物质的饱和溶液升温到t3℃,AB的溶解度变大,溶液中溶质、溶剂质量不变、溶质质量分数不变,与升温前相同,C的溶解度减小,析出晶体,溶质质量分数减小;饱和溶液中溶质的质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,即溶解度大则溶质的质量分数大,而升温前B的溶解度大于A的溶解度大于升温后C的溶解度,故溶液溶质质量分数由大到小关系是B>A>C;
故答案为:(1)A=B>C;(2)饱和;75; (3)蒸发结晶;(4)升温;(5)B>A>C.
点评 明确溶解度概念、溶解度曲线的意义、提纯物质的方法、饱和溶液与不饱和溶液的转化方法等知识,才能结合题意灵活解答,能较好考查学生分析、解决问题的能力.

练习册系列答案
相关题目
1.在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和氢氧化钠溶液中,观察到以下异常实验现象:
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
【提出问题】实验①中蓝色沉淀为什么消失?
【查阅资料】
Ⅰ.氢氧化铜在室温下温度,70℃~80℃时分解生成氧化铜.
Ⅱ.铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
Ⅰ.蓝色沉淀消失可能是氢氧化铜发生分解反应.
Ⅱ.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液.
甲同学认为猜想Ⅰ不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
乙同学为验证猜想Ⅱ,进行了如下实验.
【进行实验】
【解释与结论】
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
【反思与评价】
丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1~6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变成黑色 |
【提出问题】实验①中蓝色沉淀为什么消失?
【查阅资料】
Ⅰ.氢氧化铜在室温下温度,70℃~80℃时分解生成氧化铜.
Ⅱ.铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
Ⅰ.蓝色沉淀消失可能是氢氧化铜发生分解反应.
Ⅱ.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液.
甲同学认为猜想Ⅰ不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
乙同学为验证猜想Ⅱ,进行了如下实验.
【进行实验】
| 实验操作 | 实验现象 |
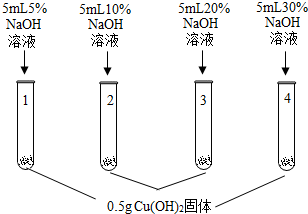 | 1号试管,… 2号试管,蓝色固体不消失 3号试管,蓝色固体减少 4号试管,蓝色固体消失,得到亮蓝色溶液 |
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
【反思与评价】
丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
5.野外生存训练课上,某同学设计了几种获得饮用水的方法,其中最不合理的是( )
| A. | 融化冰雪,煮沸后使用 | |
| B. | 收集雨水,煮沸后使用 | |
| C. | 用沙子和木炭处理海水,煮沸后使用 | |
| D. | 过滤泥水,煮沸后使用 |
2.下列物质属于纯净物的是( )
| A. | 空气 | B. | 海水 | C. | 豆浆 | D. | 水银 |
9.下列溶液暴露在空气中,因变质使溶液质量增大的是( )
| A. | 澄清石灰水 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 烧碱溶液 |
6.“水,不久将成为一个深刻的社会危机”,下列关于水资源的保护,叙述不正确的是( )
| A. | 推动世界各国对水资源进行综合性统筹规划和管理 | |
| B. | 用喷灌、滴灌方法给农作物浇水 | |
| C. | 设法提高工业用水的重复利用率 | |
| D. | 大量开采地下水以满足社会对水的需求 |
7.下列性质属于金属共同的物理性质的是( )
| A. | 硬度很大、熔点很高 | B. | 常温下都是银白色固体 | ||
| C. | 能与酸反应产生氢气 | D. | 能够导电、能够导热 |
 A、B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变,试推断:
A、B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变,试推断: