题目内容
12.实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷(CH4)气体,甲烷是一种无色 无味、密度比空气小、极难溶于水的气体.制甲烷时,气体的发生装置是A,气体的收集装置可选用E,制取好的该气体应倒(填“正”或“倒”)放在实验台上.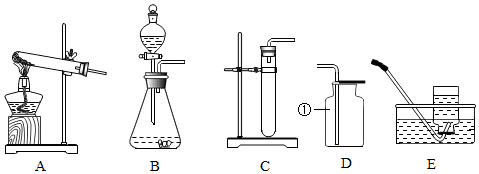
分析 题目给出有关气体的信息,根据给出的信息结合气体制备的有关内容进行分析和解答即可.
解答 解:实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷(CH4)气体,这说明是固体加热制备气体,而给定的发生装置中只有A有酒精灯,且试管口向下倾斜,所以发生装置选A.收集装置的选择要考虑密度和溶解性,由于该气体极难溶于水,所以可以用排水法收集,即收集装置可以选E.该气体密度比空气小,也可以采用向下排空气法,给定装置没涉及到.由于气体密度小于空气,所以收集好的气体应该倒放在实验台上.
故答案为:A; E;倒
点评 给定气体的有关信息,进行实验室制取收集研究,要注意信息与对应问题的有效对接,避免盲目性.

练习册系列答案
相关题目
16.下列化学用语与含义不相符的是( )
| A. | 2O--2个氧原子 | B. | Al3+--氯离子 | ||
| C. | 2H2O--2个水分子 | D. | $\stackrel{-2}{O}$--氧元素的化合价为-2价 |
3. 牛奶是我们日常生活中一种营养丰富的饮品,每天饮用可补充人们对钙等营养物质的需求.其中营养成分的具体含量如下表所示.牛奶营养成分表
牛奶是我们日常生活中一种营养丰富的饮品,每天饮用可补充人们对钙等营养物质的需求.其中营养成分的具体含量如下表所示.牛奶营养成分表
请根据资料回答下列问题:
(1)牛奶中的钙主要以磷酸钙[Ca3(PO4)2]的形式存在,它磷酸钙的相对分子质量为310,其计算式为40×3+(31+16×4)×2.
(2)磷酸钙中钙、磷、氧三种元素的质量比为60:31:64;其中钙元素的质量分数为38.7%(计算结果保留至0.1%).
(3)通常中学生每天需从牛奶中补充550mg的钙,若一盒牛奶为250mL,则理论上每天应喝2盒牛奶.
 牛奶是我们日常生活中一种营养丰富的饮品,每天饮用可补充人们对钙等营养物质的需求.其中营养成分的具体含量如下表所示.牛奶营养成分表
牛奶是我们日常生活中一种营养丰富的饮品,每天饮用可补充人们对钙等营养物质的需求.其中营养成分的具体含量如下表所示.牛奶营养成分表| 项目 | 每100mL |
| 能量 | 272kJ |
| 蛋白质 | 3.2g |
| 脂肪 | 3.8g |
| 碳水化合物 | 4.5g |
| 钠 | 60mg |
| 钙 | 110mg |
| 非脂乳固体 | ≥8.1% |
(1)牛奶中的钙主要以磷酸钙[Ca3(PO4)2]的形式存在,它磷酸钙的相对分子质量为310,其计算式为40×3+(31+16×4)×2.
(2)磷酸钙中钙、磷、氧三种元素的质量比为60:31:64;其中钙元素的质量分数为38.7%(计算结果保留至0.1%).
(3)通常中学生每天需从牛奶中补充550mg的钙,若一盒牛奶为250mL,则理论上每天应喝2盒牛奶.
4. 如图是某化学反应的模型示意图,从该图中获得的信息错误的是( )
如图是某化学反应的模型示意图,从该图中获得的信息错误的是( )
 如图是某化学反应的模型示意图,从该图中获得的信息错误的是( )
如图是某化学反应的模型示意图,从该图中获得的信息错误的是( )| A. | 反应前后元素种类改变了 | B. | 一个乙分子中含4个A原子 | ||
| C. | 该反应属于分解反应 | D. | 反应前后分子种类改变了 |
1.下列对宏观现象的微观解释不正确的是( )
| A. | 稀硫酸和稀盐酸化学性质相似也存在差异,是因为溶液中都含有H+,也存在不同的SO42-、Cl-等离子 | |
| B. | 氢氧化钠溶液与氢氧化钾溶液都能是酚酞溶液变成红色,是因为它们的溶液中都含有OH- | |
| C. | 镁和盐酸反应,从微观上看该反应实质上是镁原子和氢离子、氯离子反应生成镁离子、氯离子和氢分子 | |
| D. | 碳酸钠和碳酸钙都能与稀盐酸反应放出气体,是因为它们都含有CO32- |
2.下列属于化学性质的是( )
| A. | 可燃性 | B. | 延展性 | C. | 挥发性 | D. | 颜色、状态 |

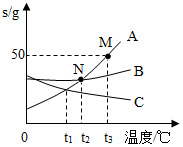 如图所示曲线A,B,C分别表示三种固体物质的溶解度变化,试回答:
如图所示曲线A,B,C分别表示三种固体物质的溶解度变化,试回答: