题目内容
2.将87.6氯化镁溶液跟一定量的氢氧化钠溶液恰好完全反应得到溶质质量分数为10%的溶液234g.求加入的氢氧化钠溶液中溶质质量分数.分析 氯化镁与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,由生成氯化钠溶液的质量、溶质的质量分数,由反应的化学方程式,列式计算出参加反应的氢氧化钠的质量、生成氢氧化镁的质量,进而计算出加入的氢氧化钠溶液中溶质质量分数.
解答 解:得到的溶质质量分数为10%的溶液234g中含氯化钠的质量为234g×10%=23.4g.
设参加反应的氢氧化钠的质量为x,生成氢氧化镁的质量为y,
2NaOH+MgCl2═Mg(OH)2↓+2NaCl
80 58 117
x y 23.4g
$\frac{80}{117}=\frac{x}{23.4g}$ x=16g
$\frac{58}{117}=\frac{y}{23.4g}$ y=11.6g
加入的氢氧化钠溶液中溶质质量分数为$\frac{16g}{234g+11.6g-87.6g}×$100%≈10.1%.
答:加入的氢氧化钠溶液中溶质质量分数为10.1%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
12.某同学拟探究物质燃烧的条件,请协助完成下列表格.
问题讨论:
(1)白磷燃烧的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)进行实验①时,如果在酒精灯上加热时间较长,蘸水的棉花球也会燃烧起来,其原因是因为加热时间过长时,水分全部被蒸发,则温度会上升至棉花的着火点,棉花就燃烧起来.
(3)实验②中利用了铜片具有导热性.
(4)实验③中做两次实验的目的是通过对比实验或对照实验.
| 实验步骤 | 实验装置图 | 实验现象 | 结论 |
| 实验①用棉花分别蘸取酒精和水,放到酒精灯火焰上加热片刻.(图1所示). | 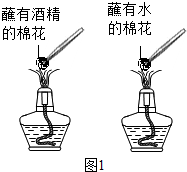 | 酒精燃烧,水没有燃烧 | 燃烧需要的条件之一是可燃物 |
| 实验②从乒乓球和滤纸上分别剪下同样大小的一小片,分别放在放在薄铜片的中部(图2所示). | 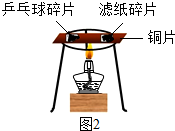 | 乒乓球片先燃烧,滤纸片后燃烧 | 燃烧需要的条件之一是温度达到着火点 |
| 实验③(1)将白磷放入8℃0热水中(图3所示). (2)将白磷放入80℃0热水中并通入氧气(图4所示). | 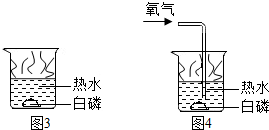 | 图3中的白磷不燃烧 图4中的白磷燃 烧 | 物质燃烧需要氧气 |
(1)白磷燃烧的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)进行实验①时,如果在酒精灯上加热时间较长,蘸水的棉花球也会燃烧起来,其原因是因为加热时间过长时,水分全部被蒸发,则温度会上升至棉花的着火点,棉花就燃烧起来.
(3)实验②中利用了铜片具有导热性.
(4)实验③中做两次实验的目的是通过对比实验或对照实验.
13.推理是一种重要的研究和学习方法.下列推理正确的是( )
| A. | 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 | |
| B. | 分子是构成物质的微粒,因此物质都是由分子构成的 | |
| C. | 碱中都含有氢氧根,所以碱中一定含有氢元素 | |
| D. | 铁丝能在氧气中燃烧,空气中有氧气,所以铁丝也能在空气中燃烧 |
10.下列能保证食品安全的是( )
| A. | 用小苏打作发酵粉焙制糕点 | B. | 用甲醛溶液浸泡海产品 | ||
| C. | 用工业石蜡给水果上蜡“美容” | D. | 用工业酒精勾兑饮用酒 |
7.下列过程直接利用太阳能的是( )
| A. | 植物生长 | B. | 火箭升空 | C. | 水电站发电 | D. | 火力发电 |
11.下列物质性质不正确的是( )
| A. | 活性炭的吸附性强 | B. | 单质碳具有还原性 | ||
| C. | 常温下碳的化学性质活泼 | D. | 石墨的导电性能好 |
3.空气质量日益成为人们关注的热点,空气质量日报主要内容包括“空气污染指数”、“空气质量级别”、“首要污染物”等.目前,计入空气污染指数项目的是( )
| A. | 二氧化碳、二氧化氮和颗粒物 | B. | 二氧化硫、二氧化氮和颗粒物 | ||
| C. | 氢气、氮气和颗粒物 | D. | 氢气、二氧化碳和颗粒物 |
