题目内容
称取一定质量的铜,放入足量稀硝酸中,反应的化学方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2R↑+4H20(R表示产生气体的化学式).用排水法收集产生的气体R,生成气体R的质量与反应时间的关系如图所示.
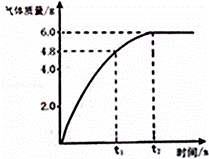
请回答下列问题:
(1)气体R的化学式是 .t1时,已反应的铜占铜的总质量的质量分数是 .
(2)称取铜的质量是多少?
考点:
根据化学反应方程式的计算.
专题:
综合计算(图像型、表格型、情景型计算题).
分析:
化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和;
化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答:
解:(1)由3Cu+8HNO3(稀)=3Cu(NO3)2+2R↑+4H20可知,反应前后铜原子个数相等,氢原子个数相等,反应后氮原子和氧原子也应该相等,因此每个R中含有1个氮原子和1个氧原子,R是一氧化氮,化学式是NO;
设t1时和t2时消耗铜的质量分别为x、y,
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H20,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H20,
192 60 192 60
x 4.8g y 6.0g
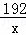 =
=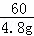 ,
,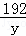 =
=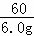 ,
,
x=15.36g,y=19.2g,
t1时,已反应的铜占铜的总质量的质量分数为: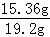 ×100%=80%,
×100%=80%,
故填:NO;80%.
(2)称取铜的质量是19.2g.
答:称取铜的质量是19.2g.
点评:
化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案下列鉴别两种不同物质的方法,不正确的是( )
| 序号 | 待鉴别的物质 | 鉴别方法 |
| A | CO2与O2 | 燃着的木条,观察燃烧情况 |
| B | 酒精与白醋 | 闻气味 |
| C | BaCO3与NaCl | 加水,观察是否溶解 |
| D | NaOH与Na2CO3 | 滴加酚酞溶液, |
| 观察溶液颜色的变化 |
尿素[CO(NH2)2]是一种常用的化学肥料,它属于( )
|
| A. | 钾肥 | B. | 磷肥 | C. | 氮肥 | D. | 复合肥 |

 燃烧
燃烧
 料
料