题目内容
10.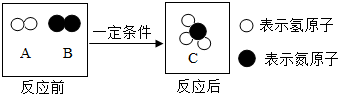 氨气在化学工业中用途广泛,合成氨反应的微观过程如图所示:则该反应中,A与B的质量比为3:14;由该图示获得的信息还有在化学变化中分子可以再分,原子不能再分(写一条即可).
氨气在化学工业中用途广泛,合成氨反应的微观过程如图所示:则该反应中,A与B的质量比为3:14;由该图示获得的信息还有在化学变化中分子可以再分,原子不能再分(写一条即可).
分析 根据合成氨反应的微观过程如图,分析反应物、生成物和反应条件书写化学方程式,由方程式求出A与B的质量比,根据微粒的变化分析分子原子变化等.
解答 解:由合成氨反应的微观过程图可知,反应物是氢气和氮气、生成物是氨气,化学方程式为:N2+3H2$\frac{\underline{\;一定条件\;}}{\;}$2NH3,则B与A的质量比为:(14×2):(3×2)=14:3;由微粒的变化可知,在化学变化中分子可以再分,原子不能再分.
故答为:3:14;在化学变化中分子可以再分,原子不能再分.
点评 此类试题属于微观粒子模型的图示题,解答时一定要弄清各微观粒子的构成情况,并能把微观粒子与宏观物质很好的联系起来,才能根据微观粒子来推测物质的种类.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
20.下列解决问题的方法可行的B
| 组别 | 要解决的问题 | 所用方法 |
| A | 鉴别二氧化碳气体和氦气 | 用燃着的小木条 |
| B | 鉴别腈纶和羊毛 | 灼烧闻气味 |
| C | 分离食盐和硝酸钾 | 溶解过滤 |
| D | 电线着火了 | 先切断电源,再进行灭火 |
15.甲、乙两化学兴趣小组用如图1所示的实验装置,通过测定产生相同体积氧气所用时间的长短来探究影响H2O2分解速率的因素.
(1)甲组:按如下设计的方案实验,请完成表1:
(2)乙组:按如下设计的方案实验,请完成表2:
(3)甲、乙两小组通过数次实验得出如图2所示的数据,请回答下列问题: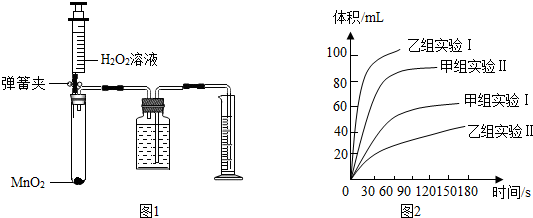
①从甲组实验得出的数据可知:H2O2浓度越大,分解速率越快.
②由乙组研究的影响H2O2分解因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;写出H2O2分解的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
【发现问题】实验开始时,H2O2溶液的温度为25℃;实验结束时,溶液的温度明显升高.说明H2O2分解是放热(选填“放热”或“吸热”)反应.
【注意:若答对第(5)小题将奖励 4分,化学卷总分不超过60分】
【反思运用】同学们经过讨论、交流和网上搜资料,提出下面两种制取H2O2液的方 法:
①用Na2O2(过氧化钠)与 H2SO4溶液作反应物,反应时将温度控制在-5~+5℃范围,生成的Na2SO4,会以
Na2SO4•10H2O晶体的形式析出,反应原理为 Na2O2+H2S04+10H2O═NaSO4•10H2O+H20,制取时Na2O2的量不能过量,因为Na2O2与水反应会生成NaOH.若Na2O2过量会造成(在碱性环境中)生成的过氧化氢分解.
②用BaO2(过氧化鋇)与H2SO4溶液作反应物.在常温下就可反应生成H2O2,试写出反应的化学方程式BaO2+H2SO4=BaSO4↓+H2O2.方法“②”比方法“①”更易操作,理由是方法①要控制好反应的温度,才能使Na2SO4•10H2O晶体析出,而方法②生成的硫酸钡是沉淀,容易与过氧化氢溶液分离.
(1)甲组:按如下设计的方案实验,请完成表1:
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| Ⅰ | 探究溶液的浓度对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 10mL 4%H2O2 |
| Ⅱ | 25℃ | 0.2gMnO2 | 10mL 8%H2O2 |
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 | 实验时溶液 酸碱度 |
| Ⅰ | 探究溶液的酸碱性 对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 0mL 8%H2O2 | pH=10.0 |
| Ⅱ | 25℃ | 0.2gMnO2 | 0mL 8%O2 | pH=4.0 |

①从甲组实验得出的数据可知:H2O2浓度越大,分解速率越快.
②由乙组研究的影响H2O2分解因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;写出H2O2分解的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
【发现问题】实验开始时,H2O2溶液的温度为25℃;实验结束时,溶液的温度明显升高.说明H2O2分解是放热(选填“放热”或“吸热”)反应.
【注意:若答对第(5)小题将奖励 4分,化学卷总分不超过60分】
【反思运用】同学们经过讨论、交流和网上搜资料,提出下面两种制取H2O2液的方 法:
①用Na2O2(过氧化钠)与 H2SO4溶液作反应物,反应时将温度控制在-5~+5℃范围,生成的Na2SO4,会以
Na2SO4•10H2O晶体的形式析出,反应原理为 Na2O2+H2S04+10H2O═NaSO4•10H2O+H20,制取时Na2O2的量不能过量,因为Na2O2与水反应会生成NaOH.若Na2O2过量会造成(在碱性环境中)生成的过氧化氢分解.
②用BaO2(过氧化鋇)与H2SO4溶液作反应物.在常温下就可反应生成H2O2,试写出反应的化学方程式BaO2+H2SO4=BaSO4↓+H2O2.方法“②”比方法“①”更易操作,理由是方法①要控制好反应的温度,才能使Na2SO4•10H2O晶体析出,而方法②生成的硫酸钡是沉淀,容易与过氧化氢溶液分离.
2.某无色溶液中,含有KNO3、BaCl2、Na2CO3、HCl中的两种物质.向混合溶液中加入稀硫酸,只看到有无色的气体产生.则此溶液中所含的物质是( )
| A. | BaCl2、Na2CO3 | B. | KNO3、HCl | C. | Na2CO3、HCl | D. | Na2CO3、KNO3 |
10.为了检测石灰石样品中碳酸钙的含量,甲、乙、丙、丁、戊五位同学分别用质量分数相同的盐酸与样品充分反应进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如表.
求:(1)碳酸钙质量分数;(计算结果精确至0.1%)
(2)稀盐酸中溶质质量分数.(计算结果精确至0.1%)
| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 所取石灰石样品的质量/g | 22 | 22 | 22 | 22 | 22 |
| 加入盐酸的质量/g | 20 | 40 | 60 | 80 | 100 |
| 烧杯内剩余物的质量/g | 39.8 | 57.6 | 75.4 | 93.2 | 93.2 |
(2)稀盐酸中溶质质量分数.(计算结果精确至0.1%)
 某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.
某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验.