题目内容
10.为了检测石灰石样品中碳酸钙的含量,甲、乙、丙、丁、戊五位同学分别用质量分数相同的盐酸与样品充分反应进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如表.| 甲 | 乙 | 丙 | 丁 | 戊 | |
| 所取石灰石样品的质量/g | 22 | 22 | 22 | 22 | 22 |
| 加入盐酸的质量/g | 20 | 40 | 60 | 80 | 100 |
| 烧杯内剩余物的质量/g | 39.8 | 57.6 | 75.4 | 93.2 | 93.2 |
(2)稀盐酸中溶质质量分数.(计算结果精确至0.1%)
分析 根据表格发现,甲、乙、丙、丁比较发现每多加入20克盐酸,烧杯内剩余物的质量减少2.2克;戊中比丁多加入20克盐酸后烧杯内剩余物的质量与丁组数据相比没有发生变化,说明盐酸过量,即丁组数据盐酸和碳酸钙恰好完全反应,生成二氧化碳的质量为8.8g,然后写出化学方程式并根据二氧化碳的质量完成解答即可.
解答 解:(1)经分析可以知道丁组数据恰好完全反应,生成二氧化碳的质量为:22g+80g-93.2g=8.8g
设碳酸钙的质量为x,80g稀盐酸中溶质的质量为y
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 73 44
x y 8.8g
$\frac{100}{x}$=$\frac{73}{y}$=$\frac{44}{8.8g}$
解得:x=20g y=14.6g
碳酸钙质量分数为:$\frac{20g}{22g}$×100%=90.9%
(2)稀盐酸中溶质质量分数为:$\frac{14.6g}{80g}$×100%=18.3%
答:(1)碳酸钙质量分数为90.9%;
(2)稀盐酸中溶质质量分数为18.3%.
点评 本题主要考查学生分析图表寻找相关信息,以及利用化学方程式进行计算的能力,能较好考查学生分析和解决实际问题的能力,是中考的常考题型.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
5.下列反应 SiO2+2C$\stackrel{高温}{→}$Si+2CO↑中,作还原剂的是( )
| A. | C | B. | CO | C. | Si | D. | SiO2 |
15.化学与生活密切相关,下列做法合理的是( )
| A. | 油锅着火用水浇灭 | B. | 电器着火用泡沫灭火器灭火 | ||
| C. | 用明火检查液化气罐是否漏气 | D. | 火场逃生时用湿毛巾捂住口鼻 |
19.从C、H、O、N、K中选择适当的元素,组成符合下列要求的物质,请用化学式进行填空;约占空气体积$\frac{1}{5}$的气体是O2;天然气的主要成分是CH4;农业上可用来作复合肥的是KNO3.
16.只发生物理变化的是( )
| A. | 活性炭吸附红墨水中的色素 | B. | 天然气燃烧 | ||
| C. | 无水硫酸铜检验水 | D. | 食物腐烂 |
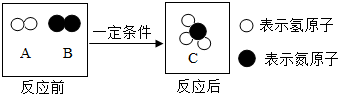 氨气在化学工业中用途广泛,合成氨反应的微观过程如图所示:则该反应中,A与B的质量比为3:14;由该图示获得的信息还有在化学变化中分子可以再分,原子不能再分(写一条即可).
氨气在化学工业中用途广泛,合成氨反应的微观过程如图所示:则该反应中,A与B的质量比为3:14;由该图示获得的信息还有在化学变化中分子可以再分,原子不能再分(写一条即可). 金属的活动性顺序是学习化学的重要工具.
金属的活动性顺序是学习化学的重要工具.
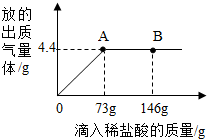 在一烧杯中盛有22.3g碳酸钠和氯化钠组成的固体混合物,加足量水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题:
在一烧杯中盛有22.3g碳酸钠和氯化钠组成的固体混合物,加足量水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答问题: