题目内容
16.向68克过氧化氢溶液中加入1克二氧化锰,至质量不再减少为止,称得剩余固体混合物的质量为67.4克.计算:(1)反应产生的氧气的质量为1.6克;
(2)计算该过氧化氢溶液中纯H2O2的质量分数?
分析 (1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.因此完全反应后,物质减少的质量就是生成的气体质量;
(2)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量,根据质量分数公式计算即可.
解答 解:(1)根据质量守恒定律,反应生成氧气的质量=68g+1.0g-67.4g=1.6g;故答案为:1.6
(2)设68.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}$=$\frac{32}{1.6g}$
x=3.4g
即:过氧化氢溶液中溶质的质量为3.4g
过氧化氢溶液的溶质的质量分数=$\frac{3.4g}{68g}$×100%=5.0%
答:过氧化氢溶液中纯H2O2的质量分数为5.0%
点评 本题主要考查学生根据质量守恒定律;运用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
7.下列关于化合价的叙述:
①化合价是元素的一种性质,因此称为元素的化合价,而不应称为原子的化合价.
②化合物中化合价有正价和负价,其数值由元素的一个原子得失电子的数目或形成共用电子对的数目决定的.
③一种元素只有一种化合价.
④在化合物中非金属元素的化合价为负值.
其中正确的是( )
①化合价是元素的一种性质,因此称为元素的化合价,而不应称为原子的化合价.
②化合物中化合价有正价和负价,其数值由元素的一个原子得失电子的数目或形成共用电子对的数目决定的.
③一种元素只有一种化合价.
④在化合物中非金属元素的化合价为负值.
其中正确的是( )
| A. | ①② | B. | ①③ | C. | ②③④ | D. | ① |
4.物质的性质决定用途.下列用途主要是利用其化学性质的是( )
| A. |  生铁制成铁锅 | B. |  金刚石作装饰品 | C. |  铜丝作导线 | D. |  氢气作高能燃料 |
8.下列一种变化与其它三种变化有本质区别,这种变化是( )
| A. | 木碳燃烧产生气体 | B. | 硫燃烧产生气体 | ||
| C. | 高锰酸钾加热产生气体 | D. | 水加热产生气体 |
6.下列混合气体点燃时可能发生爆炸的是( )
| A. | 一氧化碳和氧气 | B. | 二氧化碳和空气 | C. | 甲烷和一氧化碳 | D. | 氢气和氮气 |
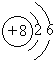 是氧原子的结构示意图,那么,1mol 氧气分子中含有9.632×1024个电子.
是氧原子的结构示意图,那么,1mol 氧气分子中含有9.632×1024个电子. 如图是某同学倾倒液体试剂的操作,请指出其中的几个错误:
如图是某同学倾倒液体试剂的操作,请指出其中的几个错误: