题目内容
20.黄铜是一种重要的金属材料,是铜和锌的合金,可以用于制造机器、电器零件及日常用品.某化学兴趣小组为了测定某黄铜样品中铜的质量分数,取10克该黄铜样品粉末放入烧杯中,再向烧杯中加入50克溶质质量分数为9.8%的稀硫酸,恰好完全反应.试求:(1)所用稀硫酸中溶质的质量;
(2)该黄铜样品中锌的质量;
(3)该黄铜样品中铜的质量分数.
分析 溶液中溶质质量=溶液质量×溶质质量分数;
锌和稀硫酸反应生成硫酸锌和氢气,根据硫酸质量可以计算锌的质量,进一步可以计算该黄铜样品中铜的质量分数.
解答 解:(1)所用稀硫酸中溶质的质量为:50g×9.8%=4.9g,
答:所用稀硫酸中溶质的质量为4.9g.
(2)设锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 98
x 4.9g
$\frac{65}{x}$=$\frac{98}{4.9g}$,
x=3.25g,
答:锌的质量为3.25g.
(3)该黄铜样品中铜的质量分数为:$\frac{10g-3.25g}{10g}$×100%=67.5%,
答:该黄铜样品中铜的质量分数为67.5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
12.造成矿难的原因之一是煤层中突然有大量瓦斯逸出,其主要成分是( )
| A. | H2 | B. | CH4 | C. | CO2 | D. | CO |
10.长期盛放石灰水的试剂瓶内壁有一层白膜,除去白膜较好的方法是( )
| A. | 用蒸馏水冲洗 | B. | 用稀硫酸洗涤 | C. | 用稀盐酸洗涤 | D. | 用热水冲洗 |
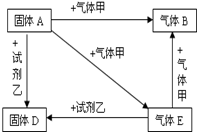 A、D是两种常见的固体,其中D为红色;B、E是两种常见的气体,其中气体E有剧毒.它们之间有如下关系:
A、D是两种常见的固体,其中D为红色;B、E是两种常见的气体,其中气体E有剧毒.它们之间有如下关系: