题目内容
14.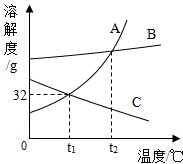 如图是A、B、C三种固体物质溶解度曲线.
如图是A、B、C三种固体物质溶解度曲线.(1)t2℃时,A、B、C三种物质溶解度由小到大的顺序是CBA;
(2)当A中有少量B时,可采用降温结晶或冷却热饱和溶液的方法提纯A;
(3)要使接近饱和的C溶液变为饱和溶液,可采用的方法是加溶质(只答一种).
(4)t1℃时,向50g水中加入20gA物质,充分溶解后所得溶液的质量是66g.
(5)将t2℃时A、B、C三种固体物质的饱和溶液降温至t1℃时,所得溶液中溶质的质量分数由小到大顺序为CAB.
分析 根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;t2℃时,A、B、C三种物质溶解度由小到大的顺序是CBA;当A中有少量B时,可采用降温结晶或冷却热饱和溶液的方法提纯A,因为A的溶解度受温度的影响变化比B大;要使接近饱和的C溶液变为饱和溶液,可采用的方法是:加溶质、蒸发水、升高温度;t1℃时,A的溶解度是32g,因此向50g水中加入20gA物质,充分溶解后所得溶液的质量=16g+50g=66g;将t2℃时A、B、C三种固体物质的饱和溶液降温至t1℃时,所得溶液中溶质的质量分数由小到大顺序为CAB,因为B析出的固体比A少,C由饱和变为不饱和,质量分数不变.
解答 解:(1)由溶解度曲线可知:t2℃时,A、B、C三种物质溶解度由小到大的顺序是CBA;故答案为:CBA;
(2)当A中有少量B时,可采用降温结晶或冷却热饱和溶液的方法提纯A,因为A的溶解度受温度的影响变化比B大;故答案为:降温结晶或冷却热饱和溶液;
(3)要使接近饱和的C溶液变为饱和溶液,可采用的方法是:加溶质、蒸发水、升高温度;故答案为:加溶质等
(4)t1℃时,A的溶解度是32g,因此向50g水中加入20gA物质,充分溶解后所得溶液的质量=16g+50g=66g;故答案为:66
(5)将t2℃时A、B、C三种固体物质的饱和溶液降温至t1℃时,所得溶液中溶质的质量分数由小到大顺序为CAB,因为B析出的固体比A少,C由饱和变为不饱和,质量分数不变;故答案为:CAB
点评 本考点考查了溶解度曲线及其应用、饱和溶液和不饱和溶液的转化等,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案| A. | NH4NO3 | B. | Ca(H2PO4)2 | C. | (NH4)2HPO4 | D. | KNO3 |
| A. | 64% | B. | 32% | C. | 80% | D. | 96% |
| A. | 秋水仙碱由碳、氢、氧三种元素组成 | |
| B. | 一个秋水仙碱分子由22个碳原子、25个氢原子、1个氮原子和3个氧分子构成 | |
| C. | 秋水仙碱分子中碳、氢、氮、氧原子个数比为22:25:1:6 | |
| D. | 秋水仙碱中氢元素的质量分数最大 |
 如图是A、B、C三种物质的溶解度曲线.下列说法错误的是( )
如图是A、B、C三种物质的溶解度曲线.下列说法错误的是( )| A. | t1℃时,A、B、C三种物质中溶解度最大的是B物质 | |
| B. | t1℃时,A、C物质饱和溶液中溶质的质量分数为20% | |
| C. | t2℃时C物质的饱和溶液不能用降温的方法转化为不饱和溶液 | |
| D. | 当A中含有少量B时,可用降温结晶的方法提纯A |
| 名称 | 符号 | 原子结构示意图 | 熔点/℃ | 沸点/℃ | 与冷水反应 |
| 锂 | Li |  | 180.5 | 1347 | 缓慢 |
| 钠 | Na |  | 97.81 | 883 | 剧烈 |
| 钾 | K |  | 63.65 | 774 | 轻微爆炸 |
| 铷 | Rb |  | 38.89 | 688 | 爆炸 |
(2)从不同方面找出对应规律(各答一点):
①原子结构从锂到铷四种元素原子的最外层电子数相同(或从上到下电子层数依次增多,从上到下第一层电子数都是2;从上到下核电荷数依次增加:从上到下电子数依次增加其他合理答案均可)
②物理性质从上到下沸点逐渐降低(或从上到下熔点逐渐降低)
③化学性质从上到下与水反应的程度越来越剧烈(或从上到下金属的活动性依次增强,合理均可).