题目内容
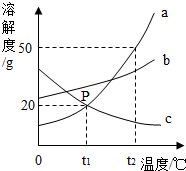 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答下列问题.
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答下列问题.(1)P点的含义是
(2)t2℃时a、b、c三种物质的溶解度按由大到小的顺序排列是
(3)浓的a溶液中混有少量b物质,要获得a物质用
(4)t2℃时30g a物质加入到50g水中不断搅拌充分溶解,形成溶液的溶质质量分数是
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,有关溶质质量分数的简单计算
专题:溶液、浊液与溶解度
分析:(1)曲线的交点表示该温度下两物质的溶解度相等;
(2)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(3)根据溶解度曲线可知物质的溶解度随温度变化情况,并分析提纯物质的方法;
(4)溶质的质量分数=
×100%.
(2)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(3)根据溶解度曲线可知物质的溶解度随温度变化情况,并分析提纯物质的方法;
(4)溶质的质量分数=
| 溶质质量 |
| 溶液质量 |
解答:解::(1)P点是t1℃时 BC两物质的 溶解度曲线的交点,表示该温度下两物质的溶解度相同;
(2)观察图示:由图中t2℃向上作纵坐标的平行线,与曲线的交点即为该温度下物质的溶解度,可知a、b、c三种物质的溶解度按由大到小的顺序排列为:a>b>c;
(3)由于a的溶解度受温度的影响较大,b的溶解度受温度影响较小,因此可以通过降温结晶或冷却热饱和溶液的方法提纯a;
(4)t2℃时,a物质的溶解度为50g,所以50g水中最多溶解25ga物质,故30ga物质加入到50g水中不断搅拌,充分溶解后形成溶液的质量是7755g,溶质的质量分数=
×100%=
×100%=33.3%.
故答案为:
(1)在t1℃时,a和c的溶解度相同; (2)a>b>c;
(3)降温结晶; (4)33.3%.
(2)观察图示:由图中t2℃向上作纵坐标的平行线,与曲线的交点即为该温度下物质的溶解度,可知a、b、c三种物质的溶解度按由大到小的顺序排列为:a>b>c;
(3)由于a的溶解度受温度的影响较大,b的溶解度受温度影响较小,因此可以通过降温结晶或冷却热饱和溶液的方法提纯a;
(4)t2℃时,a物质的溶解度为50g,所以50g水中最多溶解25ga物质,故30ga物质加入到50g水中不断搅拌,充分溶解后形成溶液的质量是7755g,溶质的质量分数=
| 溶质质量 |
| 溶液质量 |
| 25 |
| 75 |
故答案为:
(1)在t1℃时,a和c的溶解度相同; (2)a>b>c;
(3)降温结晶; (4)33.3%.
点评:本题考查固体物质的溶解度都是随温度的升高而增大,根据溶解度受温度的形象大小,确定提纯的方法,及溶液质量的简单计算.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
下列物质露置于空气中,一段时间后,质量减小的是( )
| A、碳酸钙 | B、浓硫酸 |
| C、浓盐酸 | D、氢氧化钠 |
 我国化学家侯德榜创立的侯氏制碱法,就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠,碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题:
我国化学家侯德榜创立的侯氏制碱法,就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠,碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题: 如图是学生经常使用的交通工具--自行车,请完成下列各题:
如图是学生经常使用的交通工具--自行车,请完成下列各题: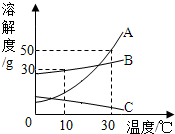 如图是A、B、C三种物质的溶解度曲线,根据如图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据如图回答下列问题: