题目内容
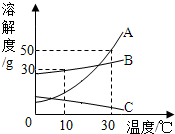 如图是A、B、C三种物质的溶解度曲线,根据如图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据如图回答下列问题:(1)30℃时向两个都盛有100g水的烧杯中,分别加入A、B 两种物质至不能溶解为止,溶液的溶质质量分数较大的是
(2)将10℃的A、B两种物质的饱和溶液降温至0℃,析出固体的质量大小是A
(3)将30℃A、B、C饱和溶液降温至10℃,所得溶液溶质质量分数由小到大的顺序是
(4)A物质的饱和溶液中含有少量B物质,通过
(5)将10℃时B物质的100g溶液恒温蒸发10g水,析出B物质的质量为
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据溶解度曲线可以比较A、B、C三种物质的溶解度大小,并分析出溶液溶质质量分数大小;
(2)不知AB饱和溶液的质量,所以无法比较析出固体的质量大小;
(3)根据固体物质的溶解度曲线比较三种物质在30℃和10℃时的溶解度大小,并结合溶液的状态转化分析解答;
(4)根据AB物质的溶解度曲线变化情况分析解答.
(3)据对应B的溶解度及溶液状态分析解答,饱和溶液中溶质的质量分数=
×100%.
(2)不知AB饱和溶液的质量,所以无法比较析出固体的质量大小;
(3)根据固体物质的溶解度曲线比较三种物质在30℃和10℃时的溶解度大小,并结合溶液的状态转化分析解答;
(4)根据AB物质的溶解度曲线变化情况分析解答.
(3)据对应B的溶解度及溶液状态分析解答,饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
解答:解:
(1)由物质的溶解度曲线可知,30℃时,A物质的溶解度大于B物质的溶解度,即30℃时100g水中溶解的A物质多.由溶质的质量分数=
×100%可知的溶质质量分数较大的是B;
故答案为:B;
(2)题目中不知AB饱和溶液的质量,所以将10℃的A、B两种物质的饱和溶液降温至0℃,无法比较析出固体的质量大小;故答案为:无法判断;
(3)30℃时,A物质的溶解度是50g,B物质的溶解度是30g,C物质的溶解度最小,降低温度至10℃,AB析出溶质,C变为不饱和溶液;观察溶解度曲线可知:10℃时的溶解度大小是C<A<B,则所得溶液溶质质量分数由小到大的顺序是C<A<B;故答案为:C<A<B;
(4)由溶解度曲线可知:A的溶解度随温度的变化比较大,B的溶解度随温度的变化比较小,所以可用冷却热饱和溶液的方法提纯其中的A物质;故答案为:冷却热饱和溶液.
(5)由图可知:对应B是的t1℃时的溶解度是30g,即10g水中最多溶解B的质量是3g,故将10℃时B物质的100g溶液恒温蒸发10g水,析出B物质的质量为 3g,B点在溶解度曲线上,为饱和溶液,剩余溶液依然是该温度下B的饱和溶液;故溶质的质量分数为:
×100%≈23%;
故答案为:
(1)B;(2)无法判断;(3)C<A<B;(4)冷却热饱和溶液.(5)3,23%
(1)由物质的溶解度曲线可知,30℃时,A物质的溶解度大于B物质的溶解度,即30℃时100g水中溶解的A物质多.由溶质的质量分数=
| 溶质的质量 |
| 溶液的质量 |
故答案为:B;
(2)题目中不知AB饱和溶液的质量,所以将10℃的A、B两种物质的饱和溶液降温至0℃,无法比较析出固体的质量大小;故答案为:无法判断;
(3)30℃时,A物质的溶解度是50g,B物质的溶解度是30g,C物质的溶解度最小,降低温度至10℃,AB析出溶质,C变为不饱和溶液;观察溶解度曲线可知:10℃时的溶解度大小是C<A<B,则所得溶液溶质质量分数由小到大的顺序是C<A<B;故答案为:C<A<B;
(4)由溶解度曲线可知:A的溶解度随温度的变化比较大,B的溶解度随温度的变化比较小,所以可用冷却热饱和溶液的方法提纯其中的A物质;故答案为:冷却热饱和溶液.
(5)由图可知:对应B是的t1℃时的溶解度是30g,即10g水中最多溶解B的质量是3g,故将10℃时B物质的100g溶液恒温蒸发10g水,析出B物质的质量为 3g,B点在溶解度曲线上,为饱和溶液,剩余溶液依然是该温度下B的饱和溶液;故溶质的质量分数为:
| 30g |
| 30g+100g |
故答案为:
(1)B;(2)无法判断;(3)C<A<B;(4)冷却热饱和溶液.(5)3,23%
点评:本题主要考查了根据固体物质的溶解度曲线解决相关的问题,同时要明确溶解度和溶质的质量分数的含义,培养了学生的分析能力和解题能力.

练习册系列答案
相关题目
下列属于化学变化的是( )
| A、利用石油中各成分的沸点不同进行石油炼制 |
| B、活性炭净水 |
| C、燃放烟花 |
| D、干冰升华 |
向物质X的水溶液中分别加入下表中的三种物质,产生的现象如下表.则物质X可能是( )
| 加入物质 | 碳酸钠溶液 | 氢氧化钡溶液 | 氧化铜粉末 |
| 现象 | 产生无色气体 | 产生白色沉淀 | 固体溶解 |
| A、HCl |
| B、CaCl2 |
| C、MgSO4 |
| D、H2SO4 |
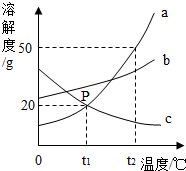 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答下列问题.
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答下列问题.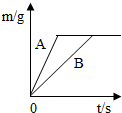 金属与我们的生活息息相关,在各个领域中用途广泛.
金属与我们的生活息息相关,在各个领域中用途广泛.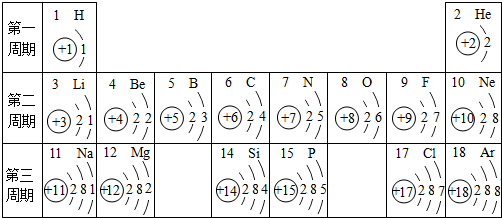
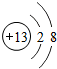 表示的是
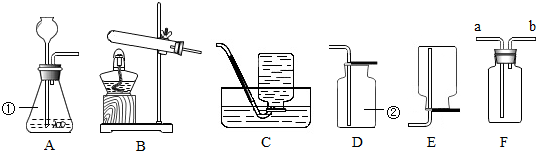
表示的是 小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图所示的两个实验:
小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图所示的两个实验: