题目内容
10. 根据如图A、B、C三种固体的溶解度曲线回答:
根据如图A、B、C三种固体的溶解度曲线回答:(1)20℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是B<A:(填写“>”、“<”或“=”)
(2)要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是降温
(3)将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是B>A>C.
(4)欲从混有少量A的B物质的饱和溶液中得到纯净的B晶体,应该采用的方法是蒸发溶剂.
分析 (1)据该温度下二者的溶解度分析解答;
(2)饱和溶液变为不饱和溶液通常可采取升温或加入溶剂的方法,并结合题意分析解答;
(3)据物质的溶解度随温度变化及饱和溶液中溶质的质量分数计算方法分析解答;
(4)据AB的溶解度手温度影响情况分析提纯物质的方法.
解答 解:(1)20℃时,B物质的溶解度大于A物质的溶解度,根据溶解度的定义可以知道欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A>B;
(2)C的溶解度随温度的升高而减小,所以要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是降低温度;
(3)将50℃时三种物质的饱和溶液分别都降温到20℃,C的溶解度随温度的升高而减小,所以降低温度对C的溶质的质量分数没有影响,据饱和时质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%可知溶解度大则溶质的 质量分数大,分析20℃时的溶解度可以知道,A的溶解度小于B的溶解度,但是大于50℃时C的溶解度,所以若将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是B>A>C;
(4)A的溶解度受温度变化影响大,而B物质的溶解度受温度变化影响较小,所以欲从混有少量B的A物质的饱和溶液中得到纯净的B晶体,应该采用蒸发结晶的方法;
(1)<;(2)降温;(3)B>A>C;(4)蒸发结晶.
点评 解答这类题目时,首先,要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的问题情景或结合所学的相关知识和技能分析解答.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
15.在一密封容器内有X、Y、Z、Q四种物质,在一定条件下充分反应后,测得反应后各物质的质量如表:
(1)反应后测得容器中物质X的质量为:55;
(2)该容器中发生的化学反应其本类型为:分解反应;请写一个和该反应类型相同的化学反应方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)该反应中物质Z与X的质量比为:84:53.
| 物质 | X | Y | Z | Q |
| 反应前质量 | 2 | 2 | 84 | 5 |
| 反应后质量 | 待测 | 24 | 0 | 14 |
(2)该容器中发生的化学反应其本类型为:分解反应;请写一个和该反应类型相同的化学反应方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)该反应中物质Z与X的质量比为:84:53.
2.下列说法中,正确的是( )
| A. | 两种或两种以上物质发生的反应叫化合反应 | |
| B. | 生成两种或两种以上其他物质的反应叫分解反应 | |
| C. | 分解反应均需加热,化合反应均需点燃 | |
| D. | 过氧化氢在二氧化锰催化作用下制取氧气的反应是分解反应 |
20.下列叙述中,不正确的是( )
| A. | 炉子上只要放一壶水就能防止煤气中毒 | |
| B. | 无铅汽油的使用可以提高城乡空气质量 | |
| C. | 使用无磷洗衣粉有利于防止水体富营养化 | |
| D. | 低碳生活有利于减缓温室效应 |
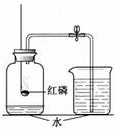 【实验探究】:空气中氧气体积含量的测定
【实验探究】:空气中氧气体积含量的测定 ,碳原子的核电荷数为6
,碳原子的核电荷数为6
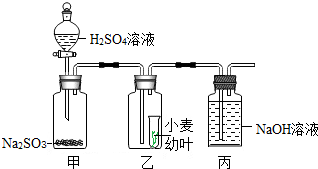 针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠反应可产生SO2气体,设计实验如图所示.
针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠反应可产生SO2气体,设计实验如图所示.