题目内容
3.请标出带点元素在化合物或原子团中的化合价.$\underset{S}{•}{{O}_{4}}^{2-}$ $\underset{S}{•}{{O}_{3}}^{2-}$ $\underset{C}{•}l{{O}_{3}}^{-}$ $\underset{N}{•}{{O}_{3}}^{-}$
$K\underset{M}{•}n{O}_{4}$ ${K}_{2}\underset{M}{•}n{O}_{4}$ $\underset{F}{•}eS{O}_{4}$ $\underset{F}{•}eC{l}_{3}$ $\underset{C}{•}a(OH)_{2}$.
分析 根据单质中元素的化合价为零;在化合物中正负化合价代数和为零进行分析解答本题.
解答 解:硫酸根中硫元素的化合价为+6价,符号为:$\stackrel{+6}{S}{{O}_{4}}^{2-}$;
亚硫酸根中硫元素的化合价为+4价,符号为:$\stackrel{+4}{S}{{O}_{3}}^{2-}$;
氯酸根中氯元素的化合价为+5价,符号为:$\stackrel{+5}{Cl}{{O}_{3}}^{-}$;
硝酸根中氮元素的化合价为+5价,符号为:$\stackrel{+5}{N}{{O}_{3}}^{-}$;
高锰酸钾中锰元素的化合价为:(+1)+a+(-2)×4=0,a=+7,符号为:$K\stackrel{+7}{Mn}{O}_{4}$;
锰酸钾中锰元素的化合价为:(+1)×2+b+(-2)×4=0,C=+6,符号为:${K}_{2}\stackrel{+6}{Mn}{O}_{4}$;
硫酸亚铁中铁元素度的化合价为+2.符号为:$\stackrel{+2}{Fe}S{O}_{4}$;
氯化铁只中氯元素的化合价为+3价,符号为:$\stackrel{+3}{Fe}C{l}_{3}$;
氢氧化钙中钙元素的化合价为+2价,符号为:$\stackrel{+2}{Ca}(OH)_{2}$;
故选答案为:+6,+4,+5,+5,+7,+6,+2,+3,+2.
点评 本题考查学生根据在化合物中正负化合价代数和为零计算指定元素化合价的解题能力.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
14.蜡烛燃烧时的火焰中,温度最高的是( )
| A. | 焰心 | B. | 内焰 | C. | 外焰 | D. | 都一样 |
18.下列说法正确的是( )
| A. | 物质的量是七个国际基本物理量之一,用“mol”表示 | |
| B. | 每摩尔任何物质都约含有6.02×1023微粒 | |
| C. | 1摩尔氧气约含有6.02×1023氧原子 | |
| D. | 1mol CO2比1mol CO多1个碳原子 |
8.在实验室制取氧气时,取MnO2和KClO3的固体混合物30.5g,加热至不再产生气体为止,收集到一定质量的氧气.某化学兴趣小组欲求所制氧气的质量,他们将加热后剩余物冷却到一定温度后,再通过多次加水测定剩余物质的办法求出,加水的质量与剩余固体质量如表:(MnO2不溶于水)
试求:(1)表中m的值为6.
(2)混合物中KClO3的质量为24.5g.
(3)所制得氧气的质量(要求写出完整的计算步骤).
| 编号 | 1 | 2 | 3 | 4 |
| 加水的质量/g | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 14.5 | 8.1 | m | 6 |
(2)混合物中KClO3的质量为24.5g.
(3)所制得氧气的质量(要求写出完整的计算步骤).
15.下列实验操作正确的是( )
| A. | 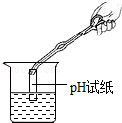 测定溶液pH值 | B. |  稀释浓硫酸 | C. |  称取食盐 | D. | 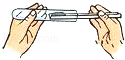 固体药品的取用 |
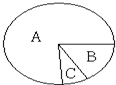
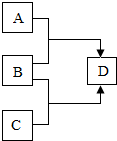 A、B、C、D为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示转化关系).
A、B、C、D为初中化学常见的物质,它们之间的转化关系如图所示(其中“→”表示转化关系).