题目内容
7.下列有关计算结果错误的是( )| A. | K2Cr2O7中Cr元素的化合价为+6价 | |
| B. | C2H4与C4H8中碳元素和氢元素的质量比相同,均为1:2 | |
| C. | NH4NO3中氮元素的质量分数为35% | |
| D. | 20℃时,NaCl的溶解度为36g,故该温度下50g水中最多溶解18g NaCl |
分析 A、根据在化合物中正负化合价代数和为零,结合K2Cr2O7的化学式进行判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据化合物中元素的质量分数公式进行分析判断.
D、根据溶解度的概念进行判断.
解答 解:A、钾元素显+1价,氧元素显-2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2x+(-2)×7=0,则x=+6价,故选项说法正确.
B、C2H4与C4H8中碳元素和氢元素的质量比分别为(12×2):(1×6)=6:1,(12×4):(1×8)=6:1,故选项说法错误.
C、NH4NO3中氮元素的质量分数为$\frac{14×2}{14×2+1×4+16×3}$×100%=35%,故选项说法正确.
D、20℃时,NaCl的溶解度为36g,是指该温度下,100g水中最多溶解36g氯化钠,故该温度下50g水中最多溶解18g 氯化钠,故选项说法正确.
故选:B.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案
相关题目
18. 某市中考化学实验操作考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小华等几位同学进行了如下图所示的实验.实验结束后,小华同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小华等几位同学对滤液的成分又进行了探究.
某市中考化学实验操作考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小华等几位同学进行了如下图所示的实验.实验结束后,小华同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小华等几位同学对滤液的成分又进行了探究.
【提出问题】滤液中除水外还含有哪些物质?
【猜想】小华认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是氢氧化钠和氢氧化钙
【讨论】你认为小华、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
【反思拓展】
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余;
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至废液呈中性.
 某市中考化学实验操作考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小华等几位同学进行了如下图所示的实验.实验结束后,小华同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小华等几位同学对滤液的成分又进行了探究.
某市中考化学实验操作考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小华等几位同学进行了如下图所示的实验.实验结束后,小华同学将①、②两支试管中的废液倒入同一个干净的烧杯中,看到废液浑浊,就对废液进行了过滤,小华等几位同学对滤液的成分又进行了探究.【提出问题】滤液中除水外还含有哪些物质?
【猜想】小华认为:只含氢氧化钠;
小明认为:可能含有氢氧化钠、碳酸钠和氢氧化钙;
小亮认为:可能含有氢氧化钠和碳酸钠;
你认为还可能是氢氧化钠和氢氧化钙
【讨论】你认为小华、小明、小亮三位同学中谁的猜想不合理,请说明理由.小明猜想不合理,因为Na2CO3和Ca(OH)2能发生反应,不能共存.
【实验设计】设计一个简单的实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,通入二氧化碳气体 | 你的猜想正确 |
①在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余;
②通过以上探究,你认为应怎样处理上述实验后的废液才能倒入下水道?在废液中加酸至废液呈中性.
15.下列相关“铁制品锈蚀的条件”的探究实验的说法中,错误的是( )


| A. | 试管中的蒸馏水可以用自来水代替 | |
| B. | 实验前要用砂纸将铁钉打磨干净 | |
| C. | 此实验中使用氯化钙的作用是吸收水蒸气 | |
| D. | 此探究应该在一周前开始做 |
12.化学课上教师演示了加热炭粉(过量)和氧化铜混合物的实验,课后课外活动小组同学对教师演示中获得的灰红色粉末样品进行实验.实验装置如图所示(图中铁架台等装置已略去,D中盛放的是固体氢氧化钠和氧化钙的混合物).
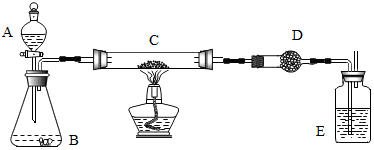
实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g.样品中铜的质量分数=$\frac{[w-(b-a)×\frac{12}{44}]}{w}$
请回答下列问题.
①主要实验内容
②实验讨论
装置E中盛放的试剂是澄清石灰水,其作用是检验D装置是否完全吸收了二氧化碳.
按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),原因是水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大,如果要得到了较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.

实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g.样品中铜的质量分数=$\frac{[w-(b-a)×\frac{12}{44}]}{w}$
请回答下列问题.
①主要实验内容
| 实验主要步骤 | 实验现象 | 有关化学方程式 |
| 打开A的上塞、活塞,慢慢滴加溶液 | B、E中有气泡 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| 对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热 | C中的灰红色粉末变成黑色 | C+O2$\frac{\underline{\;点燃\;}}{\;}$ CO2 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
装置E中盛放的试剂是澄清石灰水,其作用是检验D装置是否完全吸收了二氧化碳.
按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),原因是水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大,如果要得到了较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.
16.某化学兴趣小组的同学对碳酸钙高温加热一段时间后剩余固体的成分进行探究.
【提出问题】加热后剩余固体的成分是什么?
【猜想与探究】
猜想一:碳酸钙全部溶解,剩余固体成分为氧化钙.
做出该猜想的依据是(用化学方程式表示)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,验证该猜想的方案为把适量固体置于试管中,滴加足量稀盐酸,不产生气泡.
猜想二:碳酸钙部分分解,剩余固体成分为碳酸钙和氧化钙.
验证该猜想的方案如表所示:
【反思与评价】你认为“猜想二”的验证方案存在(填“存在”或“不存在”)问题,理由是氧化钙和水反应生成氢氧化钙,氢氧化钙微溶于水.
【提出问题】加热后剩余固体的成分是什么?
【猜想与探究】
猜想一:碳酸钙全部溶解,剩余固体成分为氧化钙.
做出该猜想的依据是(用化学方程式表示)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,验证该猜想的方案为把适量固体置于试管中,滴加足量稀盐酸,不产生气泡.
猜想二:碳酸钙部分分解,剩余固体成分为碳酸钙和氧化钙.
验证该猜想的方案如表所示:
| 实验步骤 | 实验现象 | 结论 | |
| 步骤A | 将加热后的固体放入水中,搅拌、静置 | 底部有大量白色不溶物 | 剩余固体中含有碳酸钙 |
| 步骤B | 取上层清液 溶液滴加无色 | 变红 | 剩余固体中含有 氧化钙 |