题目内容
2.(1)按照要求写出下列物质的化学式氮气N2;氖气Ne;二氧化碳CO2;红磷P;金属
锌Zn;四氧化三铁Fe3O4;二氧化锰MnO2;水H2O;氨气NH3;
硫酸H2SO4;碳酸钠Na2CO3;高锰酸钾KMnO4.
(2)写出下列各符号中数字“2”的意义
2H氢原子的个数为2个;H2一个氢分子中含有2个氢原子;2CO一氧化碳分子的个数为2;$\stackrel{+2}{CuO}$在氧化铜中铜元素显+2价;.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)氮气是由双原子分子构成的,其化学式为:N2;
氖是稀有气体元素,由稀有气体元素组成的单质是单原子分子,所以氖气的化学式就是表示氖元素的元素符号,即:Ne;
二氧化碳的化学式为:CO2;
红磷是固态非金属,由原子直接构成,其化学式为:P;
金属锌是由原子直接构成,其化学式为:Zn;
四氧化三铁的化学式为:Fe3O4;
二氧化锰的化学式为:MnO2;
水的化学式为:H2O;
氨气的化学式为:NH3;
硫酸的化学式为:H2SO4;
碳酸钠的化学式为:Na2CO3;
高锰酸钾的化学式为:KMnO4;
(2)元素符号前面的数字表示原子的个数,故2H中的2表示氢原子的个数为2个;
元素符号右下角的数字表示一个分子中的原子个数,故H2中的2表示一个氢分子中含有2个氢原子;
化学式前面的数字表示分子的个数,故2CO中的2表示一氧化碳分子的个数为2;
元素符号正上方的数字表示元素的化合价,故$\stackrel{+2}{Cu}$O中的2表示在氧化铜中铜元素显+2价;
故答案为:(1)N2;Ne;CO2;P;Zn;Fe3O4;MnO2;H2O;NH3;H2SO4;Na2CO3;KMnO4;(2)氢原子的个数为2个;一个氢分子中含有2个氢原子;一氧化碳分子的个数为2;在氧化铜中铜元素显+2价;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
12.下列选项属于可再生资源的是( )
| A. | 石油 | B. | 煤炭 | C. | 天然气 | D. | 沼气 |
7.下列有关计算结果错误的是( )
| A. | K2Cr2O7中Cr元素的化合价为+6价 | |
| B. | C2H4与C4H8中碳元素和氢元素的质量比相同,均为1:2 | |
| C. | NH4NO3中氮元素的质量分数为35% | |
| D. | 20℃时,NaCl的溶解度为36g,故该温度下50g水中最多溶解18g NaCl |
14.我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献.用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验.
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(1)分析滴加的CaCl2溶液要过量的原因:产生白色沉淀与碳酸钠充分反应;
(2)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.称得沉淀物的质量为10g
(已知 Na2CO3和CaCO3的相对分子质量分别为106和100),计算Na2CO3的质量分数为91.4%.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).
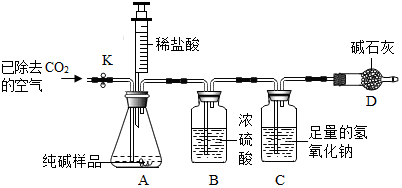
(3)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D.
(4)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(5)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据质量守恒定律,装置C(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应.
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取11.6g纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式 Na2CO3+CaCl2═CaCO3↓+2NaCl |
(2)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量.称得沉淀物的质量为10g
(已知 Na2CO3和CaCO3的相对分子质量分别为106和100),计算Na2CO3的质量分数为91.4%.
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).

(3)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D.
(4)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(5)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿.根据质量守恒定律,装置C(填标号)在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数.若没有装置D,将会使测定结果偏大(选填“偏大”或“偏小”).
11.“好一朵美丽的茉莉花…”这首歌唱出了茉莉花的美丽、芳香.在茉莉花的附近就能闻到花香,说明了( )
| A. | 分子在不断地运动 | B. | 分子可以再分 | ||
| C. | 分子间有一定的间隔 | D. | 分子的体积和质量都很小 |