题目内容
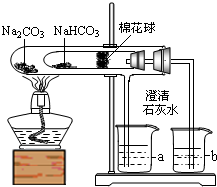 (1)某化学兴趣小组的同学对厨房中的常见物质一一小苏打(NaHCO3)的性质进行了如下实验探究:通过查阅资料,大家采用了图示装置对小苏打和纯碱的性质做对比实验.大试管为具有支管的具支试管,导管通入a烧杯;小试管用带有导管的橡皮塞,导管通入b烧杯.一段时间后,小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,b烧杯中出现了白色浑浊,a烧杯中无明显现象.冷却后,向小试管中加入稀盐酸,产生的气体使澄清石灰水变浑浊.
(1)某化学兴趣小组的同学对厨房中的常见物质一一小苏打(NaHCO3)的性质进行了如下实验探究:通过查阅资料,大家采用了图示装置对小苏打和纯碱的性质做对比实验.大试管为具有支管的具支试管,导管通入a烧杯;小试管用带有导管的橡皮塞,导管通入b烧杯.一段时间后,小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,b烧杯中出现了白色浑浊,a烧杯中无明显现象.冷却后,向小试管中加入稀盐酸,产生的气体使澄清石灰水变浑浊.
试回答:①小试管中发生的反应为______;
②在实验结束时,先后操作上要注意的是______;
③请推理这一实验中小苏打与纯碱的热稳定性的强弱顺序是:______大于______.
(2)请你根据下图,回答以下问题.
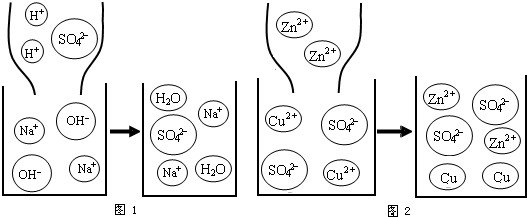
①稀硫酸和氢氧化钠溶液发生反应的微观过程如图1所示.从粒子的角度具体分析该反应能发生的原因是:______.
②锌和硫酸铜溶液发生反应的微观过程如图2所示.从粒子的角度分析该反应的实质是:______.
解:(1)无水硫酸铜粉末的棉花球变成蓝色,说明有水生成,a烧杯中石灰水无明显现象,b烧杯中石灰水了现白色浑浊,说明a中无二氧化碳生成,而b中有二氧化碳生成,即得出碳酸氢钠受热会分解,碳酸钠受热不分解(或碳酸钠比碳酸氢钠稳定)的结论,冷却后,向小试管中加入稀盐酸,产生的气体使澄清石灰水变浑浊,可得出反应后的生成物是碳酸钠;为了防止倒吸引起试管炸裂,应先将导管从烧杯中取出,再熄灭酒精灯;
(2)①变化前的微粒有:H+、SO42-、Na+、OH-,而反应后的微粒有:H2O、Na+、SO42-,则可判断反应实际上是H+与OH-反应生成H2O分子;
故答案为:氢离子和氢氧根离子反应生成了水分子;
②离子生成分子或原子变成离子或离子变成原子都可使化学变化发生,所以,化学变化就是生成新分子或新原子或新离子的变化,观察图示可知:变化前的微粒有:Zn、SO42-、Cu2+,而反应后的微粒有:Cu、SO42-、Zn2+,则可判断反应实际上是Zn→Zn2+、Cu2+→Cu的过程;
故答案为:
(1)①2NaHCO3 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
②先把导管从烧杯中取出,再熄灭酒精灯;
③碳酸钠、碳酸氢钠;
(2)①氢离子和氢氧根离子反应生成了水分子;
②反应前的锌原子和铜离子变成了锌离子和铜原子.
分析:(1)依据反应现象推测生成物,从而确定化学反应的方程式;从化学实验的基本操作以及防止倒吸的原理角度来考虑注意事项,并且由实验的现象细心分析二者的热稳定性
(2)酸碱中和反应的本质是氢离子和氢氧根离子结合成水,分析变化前后的微观过程图,从粒子的角度解释所发生的变化原因,并总结成规律.
点评:本题是结合实验和具体的图示,考查碳酸氢钠的不稳定性和通过微观图示分析溶液中发生化学变化的实质及相关基本操作,考查了学生利用课本知识结合新信息处理问题的能力.
(2)①变化前的微粒有:H+、SO42-、Na+、OH-,而反应后的微粒有:H2O、Na+、SO42-,则可判断反应实际上是H+与OH-反应生成H2O分子;
故答案为:氢离子和氢氧根离子反应生成了水分子;
②离子生成分子或原子变成离子或离子变成原子都可使化学变化发生,所以,化学变化就是生成新分子或新原子或新离子的变化,观察图示可知:变化前的微粒有:Zn、SO42-、Cu2+,而反应后的微粒有:Cu、SO42-、Zn2+,则可判断反应实际上是Zn→Zn2+、Cu2+→Cu的过程;
故答案为:
(1)①2NaHCO3
 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;②先把导管从烧杯中取出,再熄灭酒精灯;
③碳酸钠、碳酸氢钠;
(2)①氢离子和氢氧根离子反应生成了水分子;
②反应前的锌原子和铜离子变成了锌离子和铜原子.
分析:(1)依据反应现象推测生成物,从而确定化学反应的方程式;从化学实验的基本操作以及防止倒吸的原理角度来考虑注意事项,并且由实验的现象细心分析二者的热稳定性
(2)酸碱中和反应的本质是氢离子和氢氧根离子结合成水,分析变化前后的微观过程图,从粒子的角度解释所发生的变化原因,并总结成规律.
点评:本题是结合实验和具体的图示,考查碳酸氢钠的不稳定性和通过微观图示分析溶液中发生化学变化的实质及相关基本操作,考查了学生利用课本知识结合新信息处理问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
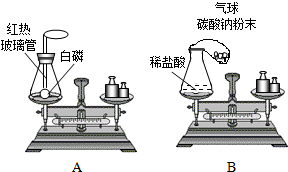
 23、请你结合下列装置图回答问题:
23、请你结合下列装置图回答问题: