题目内容
9.在置换反应A+B─→C+D中①若D为H2,则化合物B的物质类别可能为酸 (选填:氧化物、酸、碱、盐,下同)
②若D为Cu,化合物B的物质类别可能为盐.
③某此非金属也有活动性顺序,已知在溶液中可发生下列反应,Cl2+2NaBr=2NaCl+Br2,Br2+2NaI=2NaBr+I2,则在Cl2、Br2、I2三种非金属中,活动性最强的是Cl2,活动性最弱的是I2.
分析 ①在金属活动性顺序中,位于氢之前的金属可与酸发生置换反应,放出氢气;
②在金属活动性顺序中,位于前面的金属能将其后面金属从其盐溶液中置换出来进行解答;
③根据非金属强的能将其后面非金属从其盐溶液中置换出来进行解答.
解答 解:①根据金属与酸类物质发生反应所需要满足的条件可知,金属A应为在金属活动性顺序中排在氢之前;如Mg+H2SO4=MgSO4+H2↑等,所以化合物B的物质类别可能为酸;故填:酸;
②若生成物D为铜,根据金属与盐溶液反应反应的规律,可判断化合物B为可溶性铜盐,如CuSO4等,发生反应的化学方程式如Fe+CuSO4=FeSO4+Cu,所以化合物B的物质类别可能为盐;故填:盐;
③非金属强的能将其后面非金属从其盐溶液中置换出来,所以在溶液中可发生下列反应,Cl2+2NaBr=2NaCl+Br2,Br2+2NaI=2NaBr+I2,则在Cl2、Br2、I2三种非金属中,活动性最强的是Cl2,活动性最弱的是I2;故填:Cl2;I2.
点评 在金属活动性顺序中,位于氢之前的金属可与酸反应放出氢气,位于前面的金属可将其后面的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
19.20℃时,KNO3的溶解度为31.6g,则下列说法中,正确的是( )
| A. | 20℃时,31.6g KNO3在100g水里充分溶解后形成的溶液一定是饱和溶液 | |
| B. | 20℃时,KNO3饱和溶液中一定溶解有31.6g KNO3 | |
| C. | 20℃,把31.6g KNO3投入100g水里,充分溶解后形成的溶液一定是饱和溶液 | |
| D. | 30℃.31.6g KNO3不可能配制成饱和溶液 |
20. 实验小组用如下的装置进行实验.
实验小组用如下的装置进行实验.
在理解上述实验的基础上,请你归纳本实验的目的:(不超过20个字)制取氧气并测量氧气的体积.
 实验小组用如下的装置进行实验.
实验小组用如下的装置进行实验.| 实 验 步 骤 | 简 答 |
| 第一步:称取3g氯酸钾与少量二氧化锰混合后放入装置①的试管中,点燃酒精灯. | 装置①的试管中发生反应的文字表达式: 氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气 |
| 第二步:加热试管一段时间后,用橡皮管连接a、b. | 刚开始加热时,排出的气体不宜立即收集,原因是收集到的气体不纯. |
| 第三步:当装置②中水面不再下降,断开a、b,移去酒精灯,将装置②中的集气瓶密封,并贴上标签备用. | |
| 第四步:读取量筒里水的体积数并记录. | 读数时,视线必须与液体凹液面的最低处保持水平. |
4.下列实验操作和数据正确合理的是( )
| A. | 用50mL量筒量取2.3mL酒精 | |
| B. | 用湿润的PH试纸测得酸雨样品的PH为5.8 | |
| C. | 不用砝码,直接用托盘天平游码称取小苏打样品4.3g | |
| D. | 量取10mL98%的浓H2SO4慢慢注入10mL水中混合均匀得20mL49%的稀H2SO4 |
14.已知某原子的核外电子数为26,中子数比质子数多4,则该原子的相对原子质量为( )
| A. | 26 | B. | 56 | C. | 82 | D. | 86 |
19.某小组对H2O2溶液制氧气进行了如下探究:
(1)实验室用H2O2溶液和MnO2制取O2的反应符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,属于分解反应(填基本反应类型).
【探究一】:探究催化剂对H2O2分解速率的影响(实验中催化剂均为0.4g,H2O2浓度均为10%,以收集10mL气体为准)该小组采用了如图所示装置进行实验,具体数据如下表:
(2)写出有标号仪器的名称:①分液漏斗;②锥形瓶.
(3)检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若水不滴下(或漏斗下管口有水柱),则气密性良好.
(4)C装置应该选择C2,理由是反应放热,长导管可以将受放热影响排入量筒中的水回吸至B中减小实验误差.
(5)原装置中的空气对实验结果有没有影响?无;
(6)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为活性炭>CuO>MnO2.
(7)为完成此探究,需要测定的数据有收集10mL氧气所需的时间.
【探究二】:探究H2O2溶液浓度对分解速率的影响(水浴温度控制在21℃,MnO2均为0.5g,H2O2溶液均为5mL,三颈瓶容积为250mL)
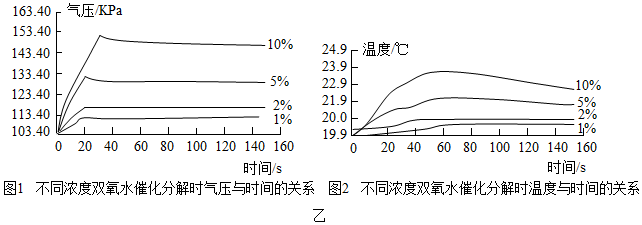
该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制如图乙图象:

(8)实验中,恒压漏斗的作用是使H2O2溶液自行下滴(使漏斗及三颈瓶成为一个整体);
(9)图1说明H2O2溶液浓度越高,反应速率越快(填“快”或“慢”),以10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;
(10)图2说明从温度看,H2O2溶液浓度越高,反应越剧烈(填“剧烈”或“平稳”).
(1)实验室用H2O2溶液和MnO2制取O2的反应符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,属于分解反应(填基本反应类型).
【探究一】:探究催化剂对H2O2分解速率的影响(实验中催化剂均为0.4g,H2O2浓度均为10%,以收集10mL气体为准)该小组采用了如图所示装置进行实验,具体数据如下表:
| 催化剂种类 | 气体产生速率(mL/s) |
| MnO2 | 0.03 |
| CuO | 0.07 |
| 活性炭 | 0.12 |
(3)检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若水不滴下(或漏斗下管口有水柱),则气密性良好.
(4)C装置应该选择C2,理由是反应放热,长导管可以将受放热影响排入量筒中的水回吸至B中减小实验误差.
(5)原装置中的空气对实验结果有没有影响?无;
(6)分析表格中数据,可以得出相同条件下表中催化剂的催化效果依次为活性炭>CuO>MnO2.
(7)为完成此探究,需要测定的数据有收集10mL氧气所需的时间.
【探究二】:探究H2O2溶液浓度对分解速率的影响(水浴温度控制在21℃,MnO2均为0.5g,H2O2溶液均为5mL,三颈瓶容积为250mL)
该小组采用了如图甲所示装置进行实验,并依据数字传感器数据绘制如图乙图象:


(8)实验中,恒压漏斗的作用是使H2O2溶液自行下滴(使漏斗及三颈瓶成为一个整体);
(9)图1说明H2O2溶液浓度越高,反应速率越快(填“快”或“慢”),以10%H2O2溶液为例,三颈瓶内气压由高缓慢降低的原因是反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;
(10)图2说明从温度看,H2O2溶液浓度越高,反应越剧烈(填“剧烈”或“平稳”).
 某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图所示).
某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图所示).