题目内容
1.通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合如图回答有关问题:
(1)图中标有a的仪器名称是铁架台.
(2)实验室用氯酸钾制取氧气,反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,欲收集较纯净的氧气,最好选用的收集装置是C (填字母,下同),判断氧气已经集满的方法是当大气泡从集气瓶口向外冒出时,证明满了.如用A装置制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)实验室用锌粒和稀盐酸制取氢气,应选择的装置组合是AC或AE,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
(4)下面图1是校本课程研究小组在老师指导下改进的电解水的实验装置示意图,下面图2是霍夫曼电解水的实验装置示意图.请据图回答下列问题:

①写出电解水的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
②用玻璃三通管将图1装置电解水时产生的气体混合在一起,点燃用该混合气吹出的肥皂泡时的实验现象是:产生剧烈爆鸣声;
③左图实验装置的优点是:仪器和装置都用生活中废旧物品制成,体现了环保与节约资源的理念,与图2装置相比,用左图装置进行该实验的主要不足之处是:硬质塑料管没有刻度,无法测量两种气体的体积比.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;排水法收集验满的方法是:当大气泡从集气瓶口向外冒出时,证明满了.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.水在通电的条件下生成氢气和氧气,配平即可;点燃用该混合气吹出的肥皂泡时的实验现象是:肥皂泡爆炸;改进实验装置的优点是:仪器和装置都用生活中废旧物品制成,体现了环保与节约资源的理念;与图2装置相比,用左图装置进行该实验的主要不足之处是:硬质塑料管没有刻度,无法测量两种气体的体积比.
解答 解:(1)铁架台是常用的夹持仪器,故答案为:铁架台;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;排水法收集验满的方法是:当大气泡从集气瓶口向外冒出时,证明满了;如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;C;当大气泡从集气瓶口向外冒出时,证明满了;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;故答案为:AC或AE;Zn+H2SO4=ZnSO4+H2↑;
(4)水在通电的条件下生成氢气和氧气,配平即可;点燃用该混合气吹出的肥皂泡时的实验现象是:肥皂泡爆炸;改进实验装置的优点是:仪器和装置都用生活中废旧物品制成,体现了环保与节约资源的理念;与图2装置相比,用左图装置进行该实验的主要不足之处是:硬质塑料管没有刻度,无法测量两种气体的体积比;故答案为:①2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;②产生剧烈爆鸣声;③仪器和装置都用生活中废旧物品制成,体现了环保与节约资源的理念;硬质塑料管没有刻度,无法测量两种气体的体积比;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满和水的电解等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH溶液(Na2SO4) | 加入适量的Ba(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | NaCl固体(Na2CO3) | 先加足量水溶解,再加适量稀盐酸,蒸发结晶 |
| D | 铜粉(铁粉) | 过量盐酸,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 英国科学家卢瑟福发现了电子,证实了原子是可分的 | |
| B. | 法国化学家拉瓦锡得出了空气是由氧气和氮气组成的结论 | |
| C. | 我国化学家侯德榜在工业制纯碱的研究中取得了巨大成就 | |
| D. | 俄国科学家门捷列夫将当时已发现的63种元素排序,制得了第一张元素周期表 |
| A. | 把TiO2加入各种酸溶液中,测量溶液的pH变化 | |
| B. | 把TiO2加入各种碱溶液中,测量溶液的pH变化 | |
| C. | 把磁铁接触TiO2后,观察TiO2是否被磁化 | |
| D. | 加热TiO2检测有无气体放出 |
| A. |  | B. |  | C. |  | D. |  |

| A. | 该反应属于置换反应 | |
| B. | 反应中甲、乙的质量比为17﹕32 | |
| C. | 甲物质含有4个原子 | |
| D. | 反应物中只有一种元素的化合价改变 |
| 选项 | 事实 | 解释 |
| A | 水烧开后易把壶盖冲起 | 温度升高,分子变大 |
| B | 金属钠与金属铝的性质不同 | 最外层电子数不同 |
| C | CO与CO2的化学性质不同 | 原子个数不同 |
| D | 金刚石与石墨的物理性质差异 | 碳原子的排列方式不同 |
 如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )| A. | A点溶液的溶质为NaOH和NaCl | B. | B点溶液的溶质只有NaCl | ||
| C. | a是NaOH溶液质量,b是稀HCl质量 | D. | 该反应是NaOH溶液滴入稀HCl中 |
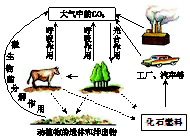 自然界就是一个天然“工厂”.自然界中的物质循环,形成了自然界中物质的平衡.如图所示为自然界中碳循环的示意.
自然界就是一个天然“工厂”.自然界中的物质循环,形成了自然界中物质的平衡.如图所示为自然界中碳循环的示意.