题目内容
4.实验室有40g碳酸银样品(杂质既不溶于水,也不与酸反应),与100g氢元素质量分数为10.5%的盐酸恰好完全反应,该样品中碳酸银的质量分数为( )| A. | 23% | B. | 46% | C. | 69% | D. | 92% |
分析 根据题干提供的信息,样品中只有碳酸银与盐酸反应,根据盐酸的质量即可求出碳酸银的质量,从而求出碳酸银的质量分数.
解答 解:100g氢元素质量分数为10.5%的盐酸,设HCl的质量为a,则有:$\frac{a×\frac{1}{36.5}+(100g-a)×\frac{2}{18}}{100g}×100%=10.5%$,a=7.3g
设碳酸银的质量为x
Ag2CO3+2HCl═2AgCl+H2O+CO2↑
276 73
x 7.3g
$\frac{276}{73}=\frac{x}{7.3g}$
x=27.6g
样品中碳酸银的质量分数为:$\frac{27.6g}{40g}×100%$=69%
故选C.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
17.日常生活中的一些小窍门或小常识往往包含着一些化学原理.下列做法正确的是( )
①油锅着火时迅速加入大量青菜灭火;
②用钢丝球擦洗铝锅上的油污;
③用汽油能除去除衣服上的油污;
④煤气泄漏及时打开换气扇排气.
①油锅着火时迅速加入大量青菜灭火;
②用钢丝球擦洗铝锅上的油污;
③用汽油能除去除衣服上的油污;
④煤气泄漏及时打开换气扇排气.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
12. 如图是某化学反应的微观模型,
如图是某化学反应的微观模型, 、
、 分别表示不同元素的原子,下列各项中,对图示模型理解正确的是( )
分别表示不同元素的原子,下列各项中,对图示模型理解正确的是( )
 如图是某化学反应的微观模型,
如图是某化学反应的微观模型, 、
、 分别表示不同元素的原子,下列各项中,对图示模型理解正确的是( )
分别表示不同元素的原子,下列各项中,对图示模型理解正确的是( )| A. | 该反应属于分解反应 | |
| B. | 该反应可能是氧化反应 | |
| C. | 在反应物和生成物中,只有一种单质 | |
| D. | 参加反应的两种物质的分子个数比为2:3 |
16.下列符号中,既可以表示一种元素,又可以表示一个原子,还可以表示一种物质的是( )
| A. | S | B. | 2C | C. | H2 | D. | O |

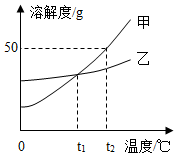 甲、乙两种物质的溶解度曲线如图所示,回答下列问题.
甲、乙两种物质的溶解度曲线如图所示,回答下列问题.