题目内容
8. 双氧水既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
双氧水既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.(1)如图,100毫升双氧水含溶质33.3克.
(2)小张用此溶液配制15%的双氧水,量水时仰视了刻度,则所配制的溶液中溶质的质量分数偏小(填“大”或“小”).
分析 (1)根据题意,密度是1.11g/mL,结合溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)量水时仰视了刻度,读数比实际液体体积小,会造成实际量取的水的体积偏大,据此进行分析解答.
解答 解:(1)100毫升双氧水含溶质的质量为1.11g/mL×100mL×30%=33.3g.
(2)量水时仰视了刻度,读数比实际液体体积小,会造成实际量取的水的体积偏大,则所配制的溶液中溶质的质量分数偏小.
故答案为:(1)33.3;(2)小.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、错误操作对溶质与溶剂的影响是正确解答此类题的关键.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
18. 研究金属与水的反应是研究金属化学性质的重要手段.较高温度下铁粉能与水蒸气反应是铁作为一种较活泼金属的有力证据.某校科学兴趣小组同学利用如图所示装置成功地完成了该实验.在高温下普通铁粉与水蒸气反应,生成铁的氧化物(与铁在氧气中的燃烧产物相同)和氢气,氢气可以在装置右端的支管处被点燃.根据以上信息回答:
研究金属与水的反应是研究金属化学性质的重要手段.较高温度下铁粉能与水蒸气反应是铁作为一种较活泼金属的有力证据.某校科学兴趣小组同学利用如图所示装置成功地完成了该实验.在高温下普通铁粉与水蒸气反应,生成铁的氧化物(与铁在氧气中的燃烧产物相同)和氢气,氢气可以在装置右端的支管处被点燃.根据以上信息回答:
(1)铁粉与水蒸气在高温下反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;其中还原剂为:铁粉.
(2)同学们对本实验成功的关键因素进行了分析:
①A处湿沙子的作用是提供水蒸汽;
②D处气体通过水的目的是 使氢气中混杂的水蒸汽遇冷液化,使氢气更纯净易于点燃.
(3)同学们还探索了铁粉用量与反应时间的关系,列表如下:(注:反应时间指加热一分钟后收集10毫升气体所需时间)从表中可以看出:铁粉用量与反应时间的关系是反应时间最短,反应速度最快.
 研究金属与水的反应是研究金属化学性质的重要手段.较高温度下铁粉能与水蒸气反应是铁作为一种较活泼金属的有力证据.某校科学兴趣小组同学利用如图所示装置成功地完成了该实验.在高温下普通铁粉与水蒸气反应,生成铁的氧化物(与铁在氧气中的燃烧产物相同)和氢气,氢气可以在装置右端的支管处被点燃.根据以上信息回答:
研究金属与水的反应是研究金属化学性质的重要手段.较高温度下铁粉能与水蒸气反应是铁作为一种较活泼金属的有力证据.某校科学兴趣小组同学利用如图所示装置成功地完成了该实验.在高温下普通铁粉与水蒸气反应,生成铁的氧化物(与铁在氧气中的燃烧产物相同)和氢气,氢气可以在装置右端的支管处被点燃.根据以上信息回答:(1)铁粉与水蒸气在高温下反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;其中还原剂为:铁粉.
(2)同学们对本实验成功的关键因素进行了分析:
①A处湿沙子的作用是提供水蒸汽;
②D处气体通过水的目的是 使氢气中混杂的水蒸汽遇冷液化,使氢气更纯净易于点燃.
(3)同学们还探索了铁粉用量与反应时间的关系,列表如下:(注:反应时间指加热一分钟后收集10毫升气体所需时间)从表中可以看出:铁粉用量与反应时间的关系是反应时间最短,反应速度最快.
| 铁粉质量/g | 0.2 | 0.4 | 0.6 | 0.8 |
| 第一次反应时间/S | 91 | 40 | 45 | 99 |
| 第二次反应时间/S | 84 | 44 | 50 | 82 |
19.如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据
(1)据如表可知二氧化锰与氯酸钾的质量比为$\frac{1}{10}$时,反应速率最快;
(2)通过分析可知,在化学反应中催化剂的用量不是越多越好.(填“是”或“不是”)
(3)二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的质量分数,所以反应速率受到影响;
(4)二氧化锰的用量过少时产生氧气的速率很慢,原因是MnO2与KClO3的接触面积小,因此催化作用不明显.
| 二氧化锰与氯酸钾的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
(2)通过分析可知,在化学反应中催化剂的用量不是越多越好.(填“是”或“不是”)
(3)二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的质量分数,所以反应速率受到影响;
(4)二氧化锰的用量过少时产生氧气的速率很慢,原因是MnO2与KClO3的接触面积小,因此催化作用不明显.
20.下列变化中,属于物理变化的是( )
| A. | 煤气燃烧 | B. | 钢铁生锈 | C. | 葡萄酿酒 | D. | 酒精挥发 |
17.小张同学用某固体物质进行如图所示的实验,根据实验判断下列说法不正确的是( )
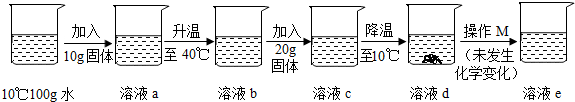

| A. | 该固体物质的溶解度随温度的升高而增大 | |
| B. | 溶液b一定是不饱和溶液 | |
| C. | 溶液d中溶质质量一定大于溶液e中的溶质质量 | |
| D. | 溶液d和溶液e的溶质质量分数可能相同 |
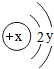
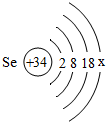 是硒的原子结构示意图,硒元素位于元素周期表的4周期、6主族.
是硒的原子结构示意图,硒元素位于元素周期表的4周期、6主族.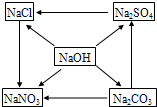 有五种化合物,它们两两之间发生的某些转化关系如图箭头所示.请回答:
有五种化合物,它们两两之间发生的某些转化关系如图箭头所示.请回答: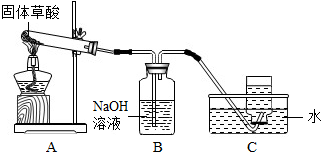 某化学课题小组通过查阅资料得知:固体草酸(H2C2O2•2H2O)受热可分解,其化学方程式(H2C2O2•2H2O═CO↑+CO2↑+3H2O)该课题小组的同学在实验室分别进行了如下实验,请回答下列问题:
某化学课题小组通过查阅资料得知:固体草酸(H2C2O2•2H2O)受热可分解,其化学方程式(H2C2O2•2H2O═CO↑+CO2↑+3H2O)该课题小组的同学在实验室分别进行了如下实验,请回答下列问题: