题目内容
11. 如图是六种物质之间的转化关系.用“一”表示两种物质之间能发生反应,用“→”表示一种物质可以转化为另一种物质.其中A、B是铁丝和氯化铜溶液中的一种,C、D是两种盐溶液(初中知识范围内).试回答下列问题:
如图是六种物质之间的转化关系.用“一”表示两种物质之间能发生反应,用“→”表示一种物质可以转化为另一种物质.其中A、B是铁丝和氯化铜溶液中的一种,C、D是两种盐溶液(初中知识范围内).试回答下列问题:(1)C与氢氧化钠溶液反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
(2)B与稀盐酸反应的现象是无明显现象.
(3)在图中写出A、B、C、D四种物质(或溶质)的化学式.
分析 根据A、B是铁丝和氯化铜溶液中的-种,A会与盐酸反应,所以A是铁,B是氯化铜,C、D是两种盐溶液,铁、氢氧化钠会与C反应,所以C是硫酸铜,D和氢氧化钠可以互相转化,所以D是碳酸钠,然后将推出的物质进行验证即可.
解答 解:(1)A、B是铁丝和氯化铜溶液中的-种,A会与盐酸反应,所以A是铁,B是氯化铜,C、D是两种盐溶液,铁、氢氧化钠会与C反应,所以C是硫酸铜,D和氢氧化钠可以互相转化,所以D是碳酸钠,经过验证,推导正确,所以A是铁,B是氯化铜,C是硫酸铜,D是碳酸钠,
(1)C与氢氧化钠溶液的反应是硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)通过推导可知,C是氯化铜,氯化铜不会与稀盐酸反应,所以B与稀盐酸反应的现象是:无明显现象;
(3)通过推导可知,A是铁,B是氯化铜,C是硫酸铜,D是碳酸钠,所以
故答案为:(1)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)无明显现象;
(3)
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
1.实验室配制一定溶质质量分数的食盐水,因疏忽导致所配溶液溶质质量分数偏低.分析以下原因,其一定不会导致这种现象发生的是( )
| A. | 量取水时,仰视量筒的读数 | |
| B. | 称量固体时,左盘放砝码,右盘放食盐 | |
| C. | 配制溶液时,烧杯原留有水 | |
| D. | 配制后的液体倾倒到细口瓶时,有一些液体溅出 |
2. 硫酸钠在不同温度时的溶解度数据如表:
硫酸钠在不同温度时的溶解度数据如表:
(1)根据所提供的溶解度数据,在图中画出硫酸钠的溶解度曲线.
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是9.5g,溶质的质量分数是8.7%精确到0.1%).
 硫酸钠在不同温度时的溶解度数据如表:
硫酸钠在不同温度时的溶解度数据如表:| 温度/℃ | 0 | 10 | 20 | 30 | 40 |
| 溶解度/g | 4.5 | 9.5 | 20.5 | 40.8 | 48.4 |
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是9.5g,溶质的质量分数是8.7%精确到0.1%).
19.关于C2H2、H2O、H2SO4三种物质的组成,叙述正确的是( )
| A. | 都含有两个氢原子 | B. | 都含有氢元素 | ||
| C. | 都含有两个氢分子 | D. | 都含有氢气 |
6.下列实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
16.下列物质的用途叙述不正确的是( )
| A. | 氢氧化钠用来治疗胃酸过多 | |
| B. | 服用鸡蛋清可以缓解重金属盐中毒 | |
| C. | 生石灰可以用作食品包装袋中的干燥剂 | |
| D. | 铵态氮肥不能和碱性物质混用 |
3.从防止空气污染的角度考虑,下列实验应在通风橱中完成的是( )
| A. |  稀释浓硫酸 | B. |  金属与酸反应 | C. |  蜡烛的熄灭 | D. |  白磷燃烧 |
1.空气中按体积分数计算含量最多的是( )
| A. | CO2 | B. | O2 | C. | N2 | D. | H2O |
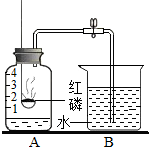 某同学用如图装置是测定空气中氧气含量的实验,先把A中水面以上分成五等份由下至上刻度分为1、2、3、4.请你填写有关空格.
某同学用如图装置是测定空气中氧气含量的实验,先把A中水面以上分成五等份由下至上刻度分为1、2、3、4.请你填写有关空格.