题目内容
6.某工厂排出的污水中可能含有Fe3+、Ba2+、K+、Na+、OH-、SO42-、Cl-、CO32-等离子,为了进一步确定,进行如下实验:(1)取污水仔细观察,呈无色透明的均一状态.
(2)取污水少许,滴入稀盐酸产生大量气泡.
由第(1)步观测可知,污水中肯定不含有的离子是Fe3+;
由第(2)步实验进一步可知,污水中肯定含有的离子是CO32-,肯定不含有的离子还有Ba2+.
分析 本题考查利用复分解反应的条件来判断物质能否共存的问题,若物质在水中解离成的离子重新结合生成水或气体或沉淀时,物质就不能共存.本题还要注意污水为无色透明溶液,则应注意常见离子在水中的颜色.
解答 解:由污水“呈无色、透明、均一状态”可知该污水中:不含Fe3+,因为三价铁离子在水溶液中呈现黄色;Ba2+与CO32-、SO42-不能共存,因为碳酸钡、硫酸钡不溶于水,会形成白色沉淀.
由“向取样的污水中,滴入稀盐酸,有大量气泡产生”可知该污水中肯定含有CO32-,因为碳酸盐遇酸能产生二氧化碳气体.肯定不含Ba2+,因为Ba2+与CO32-不能共存,SO42-无法判断是否存在.
故答案为:Fe3+,CO32-,Ba2+.
点评 本题考查了常见离子的共存问题,完成此题,可以依据复分解反应的条件进行.

练习册系列答案
相关题目
1.分析下列化肥的组成,你认为属于复合肥料的是( )
| A. | NH4HCO3 | B. | K3PO4 | C. | K2SO4 | D. | NH4Cl |
19.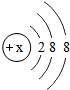 有几种元素的微粒的最外电子层结构如图所示,其中:
有几种元素的微粒的最外电子层结构如图所示,其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒符号是Ar.
(2)某微粒的盐溶液,加入AgNO3溶液时会出现白色浑浊,这种微粒符号是Cl-.
 有几种元素的微粒的最外电子层结构如图所示,其中:
有几种元素的微粒的最外电子层结构如图所示,其中:(1)某电中性微粒一般不和其他元素的原子反应,这种微粒符号是Ar.
(2)某微粒的盐溶液,加入AgNO3溶液时会出现白色浑浊,这种微粒符号是Cl-.
11.世界万物都在变化.如图所示的变化属于化学变化的是 ( )
| A. |  湿衣服晾干 | B. |  带火星木条复燃 | C. |  食盐水的蒸发 | D. |  灯泡通电发光 |
16.已知下列四个反应在一定条件下都能发生,其中属于化合反应的是( )
| A. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | |
| B. | 锌+硫酸铜→硫酸锌+铜 | |
| C. | 氢气+氯气$\stackrel{点燃}{→}$氯化氢 | |
| D. | 大理石+稀盐酸→氯化钙+二氧化碳+水 |
 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是B.
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,下面从该图获取的信息中,正确的是B.