题目内容
7.在天平两边的托盘上各放上一个盛有98克溶质质量分数为10%的硫酸的烧杯,此时天平是平衡的.现将一定量的两种物质分别加入烧杯中,两烧杯中的反应都恰好完全反应,此时天平仍保持平衡,则加入的物质可能是( )| A. | Zn和ZnO | B. | ZnO和Zn(OH)2 | C. | ZnO和ZnCO3 | D. | Zn和ZnCO3 |
分析 要使天平仍保持平衡,则加入的物质进行反应后溶液增加的质量相等,才能使天平仍能保持平衡,可以用差量法分析.
解答 解:根据题意,加入的各一定量的两种物质,都恰好完全反应,则硫酸都恰好反应,观察下列方程式,可以发现1分子的硫酸分别消耗氧化锌、碳酸锌、锌、氢氧化锌各一分子.
化学反应方程式 溶液增加的质量
ZnO+H2SO4=ZnSO4+H2O
81 81
ZnCO3+H2SO4=ZnSO4+H2O+CO2↑
125 44 125-44=81
Zn+H2SO4=ZnSO4+H2↑
65 2 65-2=63
Zn(OH)2+H2SO4=ZnSO4+2H2O
95 95
通过以上计算可以看出:氧化锌和碳酸锌分别与硫酸反应后使溶液增加的质量相等.
故选C.
点评 本题主要考查天平平衡问题结合有关化学方程式的计算,解答的关键是计算出反应后溶液增加的质量,可以利用差量法来计算,从而使本题的计算简化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15. 合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据:
合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据:
①铅锡合金中某种金属的质量分数与合金的熔点有如图所示的关系,其中横坐标表示的是锡的质量分数;当合金熔点最低时,合金中锡与铅的质量比为2:3.
②保险丝由铋、铅、锡、镉组成,其熔点约为B:
A.15~30℃B.60~80℃C.235~250℃D.300~320℃
 合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据:
合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据:| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
②保险丝由铋、铅、锡、镉组成,其熔点约为B:
A.15~30℃B.60~80℃C.235~250℃D.300~320℃
19. 你玩过“盖房子”的游戏吗?如图所示,游戏规则是根据“上下相邻的物质间均可发生化学反应,且左边上下相邻物质间反应均有沉淀生成,右边上下相邻物质间反应均有气体产生”来堆物质.根据上述游戏规则适合图中②④⑥三处物质是( )
你玩过“盖房子”的游戏吗?如图所示,游戏规则是根据“上下相邻的物质间均可发生化学反应,且左边上下相邻物质间反应均有沉淀生成,右边上下相邻物质间反应均有气体产生”来堆物质.根据上述游戏规则适合图中②④⑥三处物质是( )
 你玩过“盖房子”的游戏吗?如图所示,游戏规则是根据“上下相邻的物质间均可发生化学反应,且左边上下相邻物质间反应均有沉淀生成,右边上下相邻物质间反应均有气体产生”来堆物质.根据上述游戏规则适合图中②④⑥三处物质是( )
你玩过“盖房子”的游戏吗?如图所示,游戏规则是根据“上下相邻的物质间均可发生化学反应,且左边上下相邻物质间反应均有沉淀生成,右边上下相邻物质间反应均有气体产生”来堆物质.根据上述游戏规则适合图中②④⑥三处物质是( )| ② | ④ | ⑥ | |
| A | Na2CO3溶液 | K2CO3溶液 | 铜 |
| B | NH4Cl溶液 | 小苏打 | 苛性钠 |
| C | CuCl2溶液 | 纯碱 | 镁 |
| D | Na2SO4溶液 | 石灰水 | 铁 |
| A. | A | B. | B | C. | C | D. | D |
16.下列“家庭小实验”能达到预期目的是( )
| A. | 用空塑料瓶、小卵石、石英砂、活性炭、蓬松棉等制作简易净水器 | |
| B. | 向洗净的碎鸡蛋壳中加入食盐水可制得二氧化碳 | |
| C. | 淬火后的钢针适合做鱼钩 | |
| D. | 用白色的冷碟子不能收集到蜡烛燃烧时生成的炭黑 |
17.如图,是A、B两种物质的溶解度曲线.下列说法正确的是( )
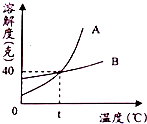

| A. | t℃时A物质饱和溶液的溶质质量分数为40% | |
| B. | B物质的溶解度受温度的影响比A物质大 | |
| C. | t℃时B物质饱和溶液降温后仍然饱和 | |
| D. | A物质的溶解度大于B物质 |
 物质A~F都是初中化学中的常见物质,它们有如图所示的转化关系.回答下列问题:
物质A~F都是初中化学中的常见物质,它们有如图所示的转化关系.回答下列问题: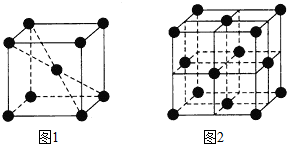 910℃以下纯铁晶体的基本结构单元如图1所示,910℃以上转变为图2所示的结构单元,在两种晶体中最邻近的铁原子间距离相同.
910℃以下纯铁晶体的基本结构单元如图1所示,910℃以上转变为图2所示的结构单元,在两种晶体中最邻近的铁原子间距离相同.