题目内容
如果配制6%的氯化钠溶液的溶质质量分数偏小,其原因是( )
| A、天平未调平衡,天平往右偏的时候放砝码并称量食盐 |
| B、转移称量好的氯化钠同体时,有少量洒落在桌面上 |
| C、俯视刻度量 |
| D、转移配制好的溶液时,有少量液体溅出 |
考点:一定溶质质量分数的溶液的配制
专题:溶液、浊液与溶解度
分析:根据溶质质量分数=
×100%,导致溶质质量分数偏小的原因有溶质的质量小了,或是溶剂的质量多了,配制好的溶液溶剂不蒸发质量分数不变等知识进行分析.
| 溶质质量 |
| 溶质质量+溶剂质量 |
解答:解:A、天平未调平衡,天平往右偏的时候放砝码并称量食盐,会导致称出的氯化钠质量偏大,导致质量分数偏大,故A错误;
B、转移称量好的氯化钠固体时,有少量洒落在桌面上,溶质的质量小了导致溶质质量分数偏小,故B正确;
C、俯视刻度读数时,读数大,实际水的体积小,导致质量分数偏大,故C错误;
D、转移配制好的溶液时,有少量液体溅出,质量分数不变,故D错误.
故选:B.
B、转移称量好的氯化钠固体时,有少量洒落在桌面上,溶质的质量小了导致溶质质量分数偏小,故B正确;
C、俯视刻度读数时,读数大,实际水的体积小,导致质量分数偏大,故C错误;
D、转移配制好的溶液时,有少量液体溅出,质量分数不变,故D错误.
故选:B.
点评:熟练掌握溶质质量分数=
×100%是解题的关键也是中考的热点.
| 溶质质量 |
| 溶质质量+溶剂质量 |

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
菊花是我国的名花.菊花中含有17种氨基酸,其中谷氨酸(化学C5H9O4N)含量较高,下列关于谷氨酸的说法正确的是( )
| A、它属于氧化物 |
| B、谷氨酸由碳原子、氢原子、氧分子、氮原子构成 |
| C、谷氨酸中碳元素、氢元素、氧元素、氮元素的质量比为5:9:4:1 |
| D、谷氨酸是由4种元素组成的化合物 |
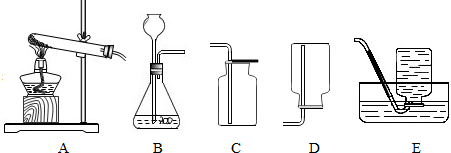
 如图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验.请完成实验报告:
如图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验.请完成实验报告:
 该粒子的质子数为
该粒子的质子数为