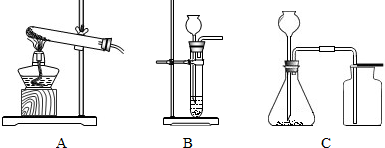
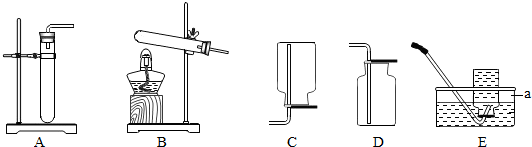
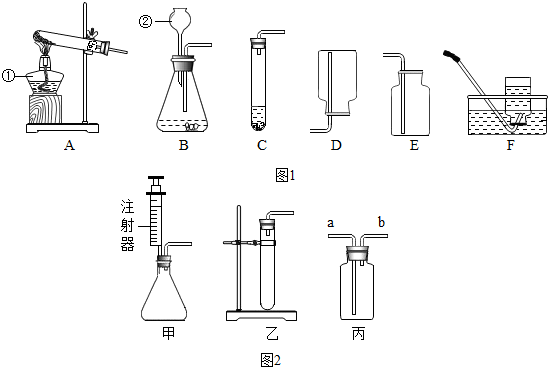
题目内容
已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①请完成证明金属粉末中存在Fe和Cu的实验设计
②化学兴趣小组的同学讨论了证明金属粉末中存在Fe和Cu的实验设计,下列他们的说法正确的是 .
A.先加氢氧化钠溶液后加稀盐酸 B.加入的溶液都要过量
C.反应过程中溶液始终是无色 D.充分反应到最后,无固体残留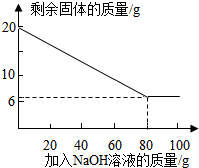
③为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:
I.分析以上数据可知,上表中n的值为 ;
Ⅱ.该金属粉末中Al的质量分数为 %
Ⅲ.列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①请完成证明金属粉末中存在Fe和Cu的实验设计
| 实验操作 | 实验现象 | 结论 |
| I.取少量的金属粉末于试管中,加入足量的 | 仅除去铝 | |
| Ⅱ.将试管静置,弃去上层清液,加入足量的稀硫酸 | 证明含有铁 | |
| Ⅲ.将试管静置,弃去上层清液,加水,多次洗涤剩余固体 | 剩余固体呈紫红色 | 证明含有铜 |
A.先加氢氧化钠溶液后加稀盐酸 B.加入的溶液都要过量
C.反应过程中溶液始终是无色 D.充分反应到最后,无固体残留

③为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如下:
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 17.3 | n | 11.9 | … |
Ⅱ.该金属粉末中Al的质量分数为
Ⅲ.列式计算:所用氢氧化钠溶液的溶质质量分数为多少?
考点:实验探究物质的组成成分以及含量,有关溶质质量分数的简单计算,金属的化学性质,根据化学反应方程式的计算
专题:科学探究
分析:(查阅资料)①I.根据已知:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,加入足量的氢氧化钠溶液,有气泡产生(或固体减少);
II.加入稀硫酸,如果有气泡产生(或固体减少或产生浅绿色溶液),则证明含有铁;
②根据铁与铜的性质分析;
③I.分析以上数据可知,第一次反应用去固体2.7克固体,第二次,也应反应掉固体2.7可,找出规律,每次减少固体2.7克,所以上表中n的值为14.6克;
II.有图中可知,剩余物质为杂质为6克,则铝的质量为(20-6)克,则该金属粉末中Al的质量分数;
III.利用化学方程式的进行计算:设氢氧化钠溶液中溶质质量分数为x,正确书写化学方程式,根据已知量和未知量,列比例式,解答,求出氢氧化钠溶液中溶质质量分数.
II.加入稀硫酸,如果有气泡产生(或固体减少或产生浅绿色溶液),则证明含有铁;
②根据铁与铜的性质分析;
③I.分析以上数据可知,第一次反应用去固体2.7克固体,第二次,也应反应掉固体2.7可,找出规律,每次减少固体2.7克,所以上表中n的值为14.6克;
II.有图中可知,剩余物质为杂质为6克,则铝的质量为(20-6)克,则该金属粉末中Al的质量分数;
III.利用化学方程式的进行计算:设氢氧化钠溶液中溶质质量分数为x,正确书写化学方程式,根据已知量和未知量,列比例式,解答,求出氢氧化钠溶液中溶质质量分数.
解答:解:(查阅资料)①I.根据已知:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,加入足量的氢氧化钠溶液,有气泡产生(或固体减少);
II.加入稀硫酸,如果有气泡产生(或固体减少或产生浅绿色溶液),则证明含有铁;
②要证明铜和铁的存在,要先将铝除尽避免干扰,先加过量的氢氧化钠溶液除去铝,后加过量的稀盐酸与铁充分反应,如果有气泡冒出,并且溶液变浅绿色,说明有铁,最后还有紫红色色固体说明有铜.故选AB
③I.分析以上数据可知,第一次反应用去2.7克固体,第二次,也应反应掉2.7克,所以上表中n的值为14.6克;
II.有图中可知,该金属粉末中Al的质量分数为
×100%=70%;
III.解:设氢氧化钠溶液中溶质质量分数为x
2Al+2H2O+2NaOH=2NaAlO2+3H2↑
54 80
2.7g 20gx
=
解得x=13.3%
答:氢氧化钠溶液中溶质质量分数为13.3%
故答为:①I.氢氧化钠溶液、有气泡产生(或固体减少);II.有气泡产生(或固体减少或产生浅绿色溶液)
②AB
③I.14.6g;II.70
III.13.3%
II.加入稀硫酸,如果有气泡产生(或固体减少或产生浅绿色溶液),则证明含有铁;
②要证明铜和铁的存在,要先将铝除尽避免干扰,先加过量的氢氧化钠溶液除去铝,后加过量的稀盐酸与铁充分反应,如果有气泡冒出,并且溶液变浅绿色,说明有铁,最后还有紫红色色固体说明有铜.故选AB
③I.分析以上数据可知,第一次反应用去2.7克固体,第二次,也应反应掉2.7克,所以上表中n的值为14.6克;
II.有图中可知,该金属粉末中Al的质量分数为
| 20g-6g |
| 20g |
III.解:设氢氧化钠溶液中溶质质量分数为x
2Al+2H2O+2NaOH=2NaAlO2+3H2↑
54 80
2.7g 20gx
| 54 |
| 2.7g |
| 80 |
| 20gx |
解得x=13.3%
答:氢氧化钠溶液中溶质质量分数为13.3%
故答为:①I.氢氧化钠溶液、有气泡产生(或固体减少);II.有气泡产生(或固体减少或产生浅绿色溶液)
②AB
③I.14.6g;II.70
III.13.3%
点评:本题主要考查了金属的化学性质和金属活动性顺序及其应用,掌握有关溶质质量分数的简单计算和根据化学方程式的计算.

练习册系列答案
相关题目
下列物质①CO2②H2O2③空气④液氧⑤河水⑥蒸馏水,其中含有氧分子的是( )
| A、①②④ | B、①②③ |
| C、③④⑤ | D、②③④ |
盛放酒精的试剂瓶标签上应印有下列警示标志中的( )
A、 |
B、 |
C、 |
D、 |
逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
| A、因为H2O和H2O2的组成元素相同,所以它们的化学性质相同 |
| B、因为化学反应通常伴随着发光、发热现象,所以有发光的变化一定是化学变化 |
| C、因为单质是由同种元素组成,所以同种元素组成的纯净物一定是单质 |
| D、因为氧气在常温常压下是无色气体,所以固态氧气也呈无色 |
如果配制6%的氯化钠溶液的溶质质量分数偏小,其原因是( )
| A、天平未调平衡,天平往右偏的时候放砝码并称量食盐 |
| B、转移称量好的氯化钠同体时,有少量洒落在桌面上 |
| C、俯视刻度量 |
| D、转移配制好的溶液时,有少量液体溅出 |