题目内容
10.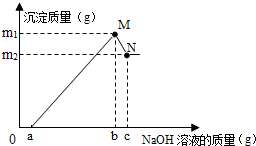 小明对废弃的易拉罐很有兴趣,为测定易拉罐中铝元素的质量分数,他剪取W克镁铝合金的易拉罐,先用过量稀硫酸溶解,然后再向溶液中滴加一定量的NaOH溶液得到氢氧化铝和氢氧化镁沉淀,继续滴加NaOH溶液时氢氧化铝被溶解[已知:Al(OH)3+NaOH═NaAlO2+XH2O],而氢氧化镁不溶于NaOH溶液,沉淀质量与滴加NaOH溶液质量关系如图所示.
小明对废弃的易拉罐很有兴趣,为测定易拉罐中铝元素的质量分数,他剪取W克镁铝合金的易拉罐,先用过量稀硫酸溶解,然后再向溶液中滴加一定量的NaOH溶液得到氢氧化铝和氢氧化镁沉淀,继续滴加NaOH溶液时氢氧化铝被溶解[已知:Al(OH)3+NaOH═NaAlO2+XH2O],而氢氧化镁不溶于NaOH溶液,沉淀质量与滴加NaOH溶液质量关系如图所示.(1)X的值为2;
(2)在a点时,溶液中的溶质除硫酸镁和硫酸铝外还有Na2SO4(填化学式);
(3)易拉罐中铝元素的质量分数为多少?(假定易拉罐只由镁和铝组成)试计算:(计算结果保留一位小数)
①反应中生成气体的质量
②样品中铝元素的质量分数.
分析 镁、铝与稀硫酸反应生成硫酸镁、硫酸铝,合金全部溶解,向所得溶液中滴加 NaOH溶液,与过量的硫酸反应生成硫酸钠,此时溶液为硫酸镁、硫酸钠、硫酸铝的混合物,继续加入氢氧化钠到增大沉淀量,金属镁离子铝离子沉淀完全,再继续加入氢氧化钠至氢氧化铝全部溶解,再加入氢氧化钠沉淀量不变.
解答 解:(1)根据质量守恒定律反应前后原子个数不变,反应前氢原子的个数是4,故2X=4,可解得X=2;
(2)在a点时,NaOH溶液恰好与过量稀硫酸反应,故此时溶液中的溶质除硫酸镁和硫酸铝外还有NaOH与稀硫酸反应生成的硫酸钠;
(3)Al的质量=$({m}_{1}-{m}_{2})×\frac{27}{27+(16+1)×3}×100%=\frac{\frac{9}{26}({m}_{1}{-m}_{2})g}{Wg}×100%=\frac{9({m}_{1}-{m}_{2})}{26W}$;
Al与H2SO4生成H2的质量为x,
2Al+3H2SO4=Al2(SO4)3+3H2↑,
54 6
$\frac{9({m}_{1}-{m}_{2})}{26}$g x
$\frac{54}{6}=\frac{\frac{9({m}_{1}-{m}_{2})}{26}g}{x}$
x=$\frac{{m}_{1}-{m}_{2}}{26}$g
Mg与H2SO4生成H2的质量为y,
Mg+H2SO4=MgSO4+H2↑,
24 2
$[W-\frac{9({m}_{1}-{m}_{2})}{26}]g$ y
$\frac{24}{2}=\frac{[W-\frac{9({m}_{1}-{m}_{2})}{26}]g}{y}$
y=$\frac{W-\frac{9({m}_{1}-{m}_{2})}{26}}{12}g$,
产生的氢气的质量为:$\frac{{m}_{1}-{m}_{2}}{26}+\frac{W-\frac{9({m}_{1}-{m}_{2})}{26}}{12}$g
样品中铝元素的质量分数为:$\frac{\frac{9({m}_{1}-{m}_{2})}{26}g}{Wg}×100%=\frac{9({m}_{1}-{m}_{2})}{26W}%$
故答案为:(1)2;
(2)Na2SO4
点评 本题考查混合物的计算,注意判断加入的NaOH溶液反应的过程,分析各过程的产物为解答该题的关键,同时考查了图象的分析应用.

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案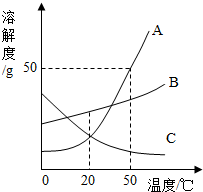 如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )| A. | 20℃时,A、B、C三种物质的溶解度由大到小的顺序是B<A=C | |
| B. | 50℃时,把50gA放人50g水中能得到A的饱和溶液 | |
| C. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 | |
| D. | 将50℃时A、B、C三种物质的饱和溶液降温到20℃时,所得溶液的溶质质量分数的大小关系是B>C=A |
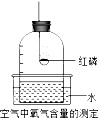
| A. | 选用红磷是因为反应可以耗尽O2,生成液态的五氧化二磷 | |
| B. | 燃烧匙中的红磷越多,水位上升越高 | |
| C. | 燃烧匙中的红磷可以换成铁丝 | |
| D. | 钟罩内气体压强的减小会导致水面的上升 |
| A. | 2Fe+3H2SO4=Fe2(SO4)3+3H2↑ | B. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | ||
| C. | CuSO4+Ba(OH)2=BaSO4↓+Cu(OH)2↓ | D. | CO+Fe2O3=Fe+CO2 |
 A-D是初中化学中常见物质,其转化关系如右图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,C、D均为黑色粉末.下列判断正确的是( )
A-D是初中化学中常见物质,其转化关系如右图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,C、D均为黑色粉末.下列判断正确的是( )| A. | A、B均为氧化物 | B. | 反应②属于置换反应 | ||
| C. | C可能是氧化铜 | D. | B可以作燃料 |
| A. | 属于氧化物 | B. | 由碳原子、氢分子和氧分子构成 | ||
| C. | 由碳、氢、氧三种元素组成 | D. | 碳、氧两种元素的质量比为76:46 |
| A. | 铁矿石 | B. | 石油 | C. | C60 | D. | 碘酒 |
| A. | 元素 | B. | 原子 | C. | 分子 | D. | 单质 |