题目内容
下列关于离子检验的说法不正确的是( )
| A、加入酸化的Ba(NO3)2溶液,出现白色沉淀,说明有SO42-存在 |
| B、加入NaOH溶液,出现红褐色沉淀,说明有Fe3+存在 |
| C、加入Ca(OH)2并用湿润的蓝色石蕊试纸检验,试纸变红,说明有NH4+存在 |
| D、加入无色酚酞,溶液变红,说明有OH-存在 |
考点:常见离子的检验方法及现象
专题:物质的检验、鉴别与推断
分析:A、根据SO32-加入酸化的Ba(NO3)2溶液会被氧化为SO42-分析;
B、根据Fe3+的检验方法分析;
C、根据NH4+的检验方法分析;
D、根据碱性溶液检验方法分析.
B、根据Fe3+的检验方法分析;
C、根据NH4+的检验方法分析;
D、根据碱性溶液检验方法分析.
解答:解:A、由于SO32-在加入酸化的Ba(NO3)2溶液中会被氧化为SO42-,会生成硫酸钡沉淀,不能说明有SO42-存在,故A错误;
B、由于Fe3+与加入NaOH溶液,会生成氢氧化铁红褐色沉淀,故B正确;
C、加入Ca(OH)2并用湿润的蓝色石蕊试纸检验,试纸变蓝,说明有NH4+存在.故C错误
D、加入无色酚酞,溶液变红,说明溶液显碱性有OH-存在.故D正确.
故选AC.
B、由于Fe3+与加入NaOH溶液,会生成氢氧化铁红褐色沉淀,故B正确;
C、加入Ca(OH)2并用湿润的蓝色石蕊试纸检验,试纸变蓝,说明有NH4+存在.故C错误
D、加入无色酚酞,溶液变红,说明溶液显碱性有OH-存在.故D正确.
故选AC.
点评:本题的难度不大,熟记常见离子的检验方法是解答本题的关键.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
2014年6月5日--世界环境日中国主题为:“向污染宣战”.下列有关环境的说法不正确的是( )
| A、雾霾是一种自然现象,对人体健康影响不大 |
| B、二氧化碳是主要的温室气体之一 |
| C、PM2.5是指大气中直径小于或等于2.5μm的颗粒物 |
| D、汽车尾气是城市空气的污染源之一 |
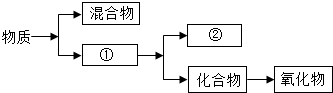 如图是关于物质的分类:
如图是关于物质的分类: