题目内容
1.向盛有2克CuO和Cu粉混合物的试管中通入氢气,将混合物加热至都变红色粉末,在氢气流中冷却后称的残余固体物的质量为1.68克,求原混合物中CuO和Cu的质量各是多少克?分析 氢气与氧化铜反应生成铜和水,由题意,反应后固体的质量减少了2g-1.68g=0.32g,据此结合固体差量法进行分析解答.
解答 解:设原混合物中CuO的质量为x
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O 固体差量
80 64 80-64=16
x 2g-1.68g=0.32g
$\frac{80}{16}=\frac{x}{0.32g}$ x=1.6g
原混合物中Cu的质量是2g-1.6g=0.4g.
答:原混合物中CuO和Cu的质量分别是1.6g、0.4g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,采用差量法是正确解答本题的捷径.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
12.2008年“世界环境日”的主题是“促进低碳经济”,提倡人们“低碳生活,绿色出行”,其中“碳”指的是…( )
| A. | C60 | B. | 木炭 | C. | 二氧化碳 | D. | 一氧化碳 |
9.某省盛产石灰石,其中含有杂质为二氧化硅(不溶水).某中学初三研究小组的同学为了测定某矿山石灰石的纯度(碳酸钙的质量分数),取4.0g该矿山石灰石样品,将50g盐酸平均分成5份,分5次加入到样品中,数据见下表:
(1)五次实验中,盐酸完全反应的有第1、2、3 次(填写实验的次数).
(2)石灰石样品中碳酸钙的质量分数.
(3)此种盐酸里的氯化氢气体的质量分数.
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入盐酸质量/g | 10 | 10 | 10 | 10 | 10 |
| 每次产生气体质量/g | 0.44 | 0.44 | 0.44 | 0.22 | 0 |
(2)石灰石样品中碳酸钙的质量分数.
(3)此种盐酸里的氯化氢气体的质量分数.
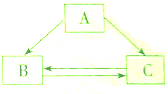 碳及其氧化物之间存在如图所示的相互转化关系,其中B是A不充分燃烧的产物.请回答下列问题:
碳及其氧化物之间存在如图所示的相互转化关系,其中B是A不充分燃烧的产物.请回答下列问题: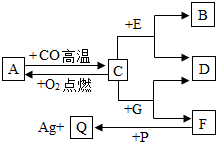 现有A、B、C、D、E、F、G、P、Q九种物质,其中A为磁铁矿的主要成分,C、F是常见金属,B是相对分子质量最小的气体单质,D为浅绿色溶液,G为蓝色溶液.它们之间关系如图所示,试推测:
现有A、B、C、D、E、F、G、P、Q九种物质,其中A为磁铁矿的主要成分,C、F是常见金属,B是相对分子质量最小的气体单质,D为浅绿色溶液,G为蓝色溶液.它们之间关系如图所示,试推测: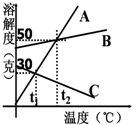 A、B、C三种物质的溶解度随温度的变化情况如图:
A、B、C三种物质的溶解度随温度的变化情况如图: