题目内容
14.下列是研究氧气、水、二氧化碳、金属性质的实验.根据图示,回答问题.
(1)A中铁丝在氧气中燃烧,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
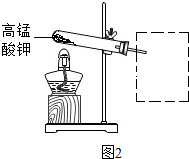
(2)B中试管a中产生的气体为O2.
(3)C中观察到的现象是蜡烛由下至上依次熄.
(4)D实验可得到的结论是Fe>Cu>Ag.
分析 (1)根据铁丝燃烧生成四氧化三铁,写出反应的方程式;
(2)分析电解水实验的示意图,观察到与电源负极相连的试管b内气体为氢气、与电源正极相连的试管a内气体为氧气解答;
(3)根据图示操作进行二氧化碳的性质;
(4)根据金属的化学性质解答.
解答 解:
(1)铁丝燃烧生成四氧化三铁,反应的方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
(2)由水通电分解的示意图可知,试管b收集的是电源的正极上产生的气体,较少,是氧气;
(3)此实验中观察到的现象是下面的蜡烛先熄灭,上面的蜡烛后熄灭,说明二氧化碳的密度比空气大,不燃烧、不支持燃烧;
(4)铁放入硫酸铜溶液中,铁丝表面有红色物质析出,说明铁的活泼性大于铜,铜放入硝酸银溶液中,铜表面有银白色物质析出,说明铜的活泼性大于银;
答案:
(1)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
(2)O2
(3)蜡烛由下至上依次熄灭
(4)金属活动性:Fe>Cu>Ag
点评 本题考查了化学实验的操作以及有关的实验结论的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列知识点的总结归纳合理的是( )
| A. | 碱溶液都能使酚酞变红,所以氢氧化铜也能使酚酞变红 | |
| B. | 有机化合物都含有碳元素,则含碳元素的化合物都是有机物 | |
| C. | 含有亚铁离子的溶液都显浅绿色,所以氯化亚铁溶液显浅绿色 | |
| D. | 碳酸盐与酸反应会有气泡产生,则与酸反应产生气泡的固体一定是碳酸盐 |
3.下列说法正确的是( )
| A. | 喝了汽水会打嗝,说明压强减小气体的溶解度增大 | |
| B. | 金刚石和石墨物理性质存在着明显差异,是因为构成它们的碳原子的排列方式不同 | |
| C. | 二氧化锰可以加快过氧化氢分解速率,所以二氧化锰可以做任何化学反应的催化剂 | |
| D. | C、H2、CO都具有还原性,在一定条件下它们都能跟氧化铁发生置换反应 |


 水是一种很好的溶剂,在生产、生活中有很重要的用途.
水是一种很好的溶剂,在生产、生活中有很重要的用途.