��Ŀ����
7��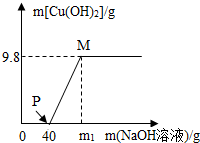 ��CuCl2��HCl��100g�����Һ�У���μ���������������Ϊ10%NaOH��Һ���μӷ�Ӧ��NaOH��Һ���������ɳ���������ϵ��ͼ����ͼ�ش�
��CuCl2��HCl��100g�����Һ�У���μ���������������Ϊ10%NaOH��Һ���μӷ�Ӧ��NaOH��Һ���������ɳ���������ϵ��ͼ����ͼ�ش���1��д��PM�η����Ļ�ѧ����ʽCuCl2+2NaOH�TCu��OH��2��+2NaCl��
��2��P����Һ�е�������CuCl2��NaCl��
��3��ԭ�������CuCl2�������Ƕ��٣�
��4����ͨ������ȷ��m1��ֵ
��5��M����Һ���������������Ƕ��٣��������0.1%��
���� ��CuCl2��HCl�Ļ����Һ����μ���NaOH��Һ�����������������ᷴӦ�����Ȼ��ƺ�ˮ������ͼ����Կ�����P��ʱ������������Һ�е�����ǡ�÷�Ӧ���ټ�����������ʱ�����������Ȼ�ͭ��Ӧ����������ͭ�������Ȼ��ƣ��������ɵ�������ͭ����������������Ȼ�ͭ����������Ӧ���������Ƶ����������ɵ��Ȼ��Ƶ����������ɽ����йصļ��㣮
��� ����𡿽⣺��1���������ͼ���֪��PM�η����ķ�Ӧ�������������Ȼ�ͭ��Ӧ������������ͭ�������Ȼ��ƣ���Ӧ��ѧ����ʽ�ǣ�CuCl2+2NaOH�TCu��OH��2��+2NaCl��
��2���������ͼ���֪��P��ʱ��������������Һ�е�����ǡ�÷�Ӧ����Һ�е������ǣ�CuCl2��NaCl��
��3����ԭ��������Ȼ�ͭ��������x�����Ȼ�ͭ��Ӧ���������Ƶ�����Ϊy�������Ȼ��Ƶ�����Ϊz
CuCl2+2NaOH�TCu��OH��2��+2NaCl
135 80 98 117
x y 9.8g z
$\frac{135}{x}=\frac{80}{y}=\frac{98}{9.8g}=\frac{117}{z}$
��ã�x=13.5g y=8g z=11.7g
��4�������������֪��m1=40g+$\frac{8g}{10%}$=120g
��5�����������������ᷴӦ���ɵ��Ȼ��Ƶ�����p
NaOH+HCl�TNaCl+H2O
40 58.5
40g��10% p
$\frac{40}{58.5}=\frac{40g��10%}{p}$ ��ã�p=5.85g
M����Һ���������������ǣ�$\frac{11.7g+5.85g}{100g+120g-9.8g}��100%$��8.3%
�ʴ�Ϊ����1��CuCl2+2NaOH�TCu��OH��2��+2NaCl��
��2��CuCl2��NaCl��
��3��ԭ�������CuCl2��������13.5g��
��4����ͨ������ȷ��m1��ֵ��120g
��5��M����Һ����������������8.3%
���� ��Һ�ͻ�ѧ��Ӧ�ںϵ���Ŀ�����ۺ��Ե����ͣ�Ҫ��Ƚϸߣ�ͨ��ѧ���ڼ���ʱ�����������ʵ�ʲμӷ�Ӧ������Һ�����ʵ����������������40gֱ�Ӵ��뻯ѧ����ʽ���м��㣮���Ҫ��ѧ���㹻ϸ�ġ��������������������

| A�� | �������ƺ�ϡ����������ɫ��Һ���ǰ�����¶ȼƹ۲��¶ȱ仯����֤���Ƿ���л�ѧ�仯 | |
| B�� | Ϊ��֤�������ڿ����е�����������Һ�Ƿֱ��ʣ�����������������Һ�е������ᣬ�۲��Ƿ������������ | |
| C�� | ����������Һ�м���һ������ϡ���ᣬ����ͨ����������FeCl3������������˵����ȫ�к� | |
| D�� | ��ϡ���������ϴ�ڱ���CaCO3���Թ� |
| A�� |  ������ | B�� |  ��ʳ�� | C�� |  �ɲ�Ҷ | D�� |  ժ��ݮ |
 ��503.2gFeCl3��CuCl2�Ļ����Һ�м������ۣ���֪��Ӧ���Ⱥ�˳��ͻ�ѧ����ʽ�ֱ�Ϊ��2FeCl3+Fe�T3FeCl2 CuCl2+Fe�TFeCl2+Cu����ͼΪ�������۵������뷴Ӧ��ʣ�����������ϵ����ش���������
��503.2gFeCl3��CuCl2�Ļ����Һ�м������ۣ���֪��Ӧ���Ⱥ�˳��ͻ�ѧ����ʽ�ֱ�Ϊ��2FeCl3+Fe�T3FeCl2 CuCl2+Fe�TFeCl2+Cu����ͼΪ�������۵������뷴Ӧ��ʣ�����������ϵ����ش���������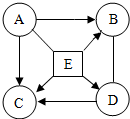 ��֪A��B��C��D��E��Ϊ���л�ѧ�������ᡢ��Ρ����������B�������C���Ȼ��ƣ�E�ڹ�ҵ�Ϲ㷺��Ӧ���ڲ�������ֽ�ȵ����������Ǵ�����ͼ��ʾ��ת����ϵ����֪A��E�ܷ�Ӧ�������壬��ش��������⣨��-����ʾ����ܷ�Ӧ����������ʾ��ij�������������ɸ����ʣ�
��֪A��B��C��D��E��Ϊ���л�ѧ�������ᡢ��Ρ����������B�������C���Ȼ��ƣ�E�ڹ�ҵ�Ϲ㷺��Ӧ���ڲ�������ֽ�ȵ����������Ǵ�����ͼ��ʾ��ת����ϵ����֪A��E�ܷ�Ӧ�������壬��ش��������⣨��-����ʾ����ܷ�Ӧ����������ʾ��ij�������������ɸ����ʣ�
