题目内容
【题目】某化学兴趣小组想要探究一包食品脱氧剂的成分,剪开包装袋,发现脱氧剂大部分为黑色固体,其中混有少量白色粉末。
[提出问题]脱氧剂的成分是什么?
[猜想与假设]经过查阅资料,小组同学提出猜想:甲同学:可能有铁粉;乙同学:可能有炭粉。
[设计实验]小组同学根据两位同学的猜想设计了实验方案,请完成下表:
实验步骤 | 实验现象 | 实验结论 |
向脱氧剂中加入足量的稀盐酸 | 固体部分溶解,有气泡产生 | 甲、乙同学的猜想均成立 |
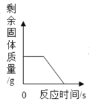
过滤,将滤渣与氧化铜混合加热 | _____ |
[反思与评价]
(1)有同学提出,可以用一种简单的物理方法验证甲同学的猜想,请写出使用此方法的实验操作及现象:_____。
(2)老师告诉同学们,脱氧剂的脱氧原理是利用铁与氧气、水反应生成氢氧化铁来吸收包装袋中氧气,从而延长食品的保质期。该反应的化学方程式是_____,所属的基本反应类型是_____
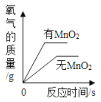
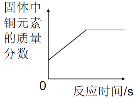
(3)小组同学又对脱氧剂中的白色粉末产生好奇,经查阅资料,白色粉末可能是硅藻土。硅藻土是一种填充剂,不溶于水,其作用在于吸附水分,为脱氧反应提供水分;并疏松配料,使氧气易于接触铁粉。如图是硅藻土用量与脱氧时间(h)的关系图,可知:
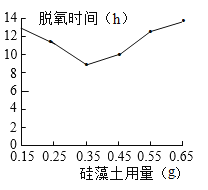
①硅藻土的最佳用量是0.35g.
②硅藻土高于或低于最佳量时,脱氧速度会减慢。请分别分析可能的原因:_____;
(4)脱氧剂的脱氧速度还有可能受哪些因素影响?请写出一条并说明理由,影响因素:_____理由:_____
【答案】黑色粉末逐渐变为红色 用磁铁靠近脱氧剂,部分黑色粉末被吸引 ![]() 化合反应 量不足时,吸收水分不足,反应不充分;量太多时,包裹在铁粉表面,使铁粉不能与氧气充分接触 温度 因为温度越高,反应速度越快
化合反应 量不足时,吸收水分不足,反应不充分;量太多时,包裹在铁粉表面,使铁粉不能与氧气充分接触 温度 因为温度越高,反应速度越快
【解析】
探究食品脱氧剂的成分。
提出问题:脱氧剂的成分是什么?
猜想与假设:
甲同学:可能有铁粉;
乙同学:可能有炭粉。
设计实验:
实验步骤:向脱氧剂中加入足量的稀盐酸
实验现象:固体部分溶解,有气泡产生
该实验现象说明甲同学的猜想成立,因为铁粉与稀盐酸反应生成氯化亚铁和氢气;
实验步骤:过滤,将滤渣与氧化铜混合加热
根据实验结论乙同学的猜想成立,即粉末中有炭粉,可以推测出
实验现象:黑色粉末逐渐变为红色
实验结论:甲、乙同学的猜想均成立
反思与评价:
(1)有同学提出,可以用一种简单的物理方法验证甲同学的猜想,因为铁粉可以被磁铁吸引,由此方法可以验证铁粉的存在,则实验操作及现象为:用磁铁靠近脱氧剂,部分黑色粉末被吸引。
(2)脱氧剂的脱氧原理是利用铁与氧气、水反应生成氢氧化铁来吸收包装袋中氧气,从而延长食品的保质期。该反应的化学方程式是![]() ,由三种物质生成一种物质,所属的基本反应类型是化合反应。
,由三种物质生成一种物质,所属的基本反应类型是化合反应。
(3)根据资料信息和硅藻土用量与脱氧时间(h)的关系图可知:
①硅藻土的最佳用量是0.35g;
②硅藻土高于或低于最佳量时,脱氧速度会减慢,可能的原因是量不足时,吸收水分不足,反应不充分;量太多时,包裹在铁粉表面,使铁粉不能与氧气充分接触。
(4)脱氧剂的脱氧速度还有可能受温度影响,因为温度越高,反应速度越快。

【题目】当把燃着的小蜡烛放入一个集气瓶中并塞紧胶塞时,蜡烛一会儿就熄灭了。那么,蜡烛为什么会熄灭呢?某化学兴趣小组进行了如下探究,请完成以下填空。
(提出猜想)
猜想1:蜡烛燃烧把集气瓶内的氧气耗尽,导致蜡烛熄灭。
猜想2:蜡烛燃烧随集气瓶内氧气含量降低而变弱,放出热量减少,使温度降至蜡烛的着火点以下,导致蜡烛熄灭。
猜想3:蜡烛燃烧产生的二氧化碳能灭火,导致蜡烛熄灭。
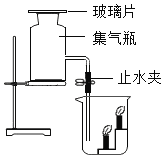
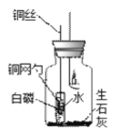
(进行实验)小组设计如下图所示的实验装置,并进行实验来验证猜想。
| 实验操作 | 实验现象 |
点燃蜡烛并连同胶塞上的其他仪器和药品一起放入集气瓶中,塞紧胶塞。 | 蜡烛火焰逐渐变弱,最终熄灭。 | |
蜡烛熄灭并静置冷却后,将铜丝上提,使盛白磷的铜网勺高于试管口,试管倒下,水流出。 | 一会儿后,白磷燃烧,有大量的____产生。 |
(分析和结论)
(1)蜡烛熄灭前,白磷要浸没在小试管所盛的水中,其目的是______。
(2)集气瓶中装入生石灰的目的是利用生石灰与水接触发生反应,其化学方程式是_____,且该反应将____(填“吸热”或“放热”),使瓶内温度升高。
(3) 瓶内的白磷能燃烧,证明猜想____和_____不成立。
(反思与交流)
(4) 通过本实验可知,燃烧的条件之一“燃烧需要氧气”这一条件应补充完善为______。