题目内容
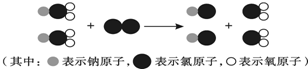
17. 如图示意图形象地表示了某化学反应前后分子的变化.其中
如图示意图形象地表示了某化学反应前后分子的变化.其中  表示氧原子、
表示氧原子、 表示碳原子,则:该反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
表示碳原子,则:该反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;该反应中各反应物、生成物微粒数目比为2:1:2.
分析 关键是根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式,根据方程式的意义分析判断反应中各反应物、生成物微粒数目比.
解答 解:由反应的微观模型图可知,该反应是一氧化碳和氧气反应生成二氧化碳,反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.由方程式可知,该反应中各反应物、生成物微粒数目比为2:1:2.
故答为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,2:1:2.
点评 解答本题的关键是要掌握化学方程式的书写方法和分子与原子在化学变化中的关系等方面的知识,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
8.某元素的化合物的化学式为R2O3,其中氧元素的质量百分含量为30%,则R的相对原子质量是( )
| A. | 27 | B. | 23 | C. | 39 | D. | 56 |
5.海湾战争引起科威特大量油井燃烧,造成严重的大气污染.据报导,有些地区降黑雨,你分析形成黑雨的主要污染成分是( )
| A. | 炭黑 | B. | 二氧化氮 | C. | 二氧化硫 | D. | 一氧化碳 |
12.下列由离子构成的物质是( )
| A. | 铜 | B. | 干冰 | C. | 氯化钠 | D. | 水 |
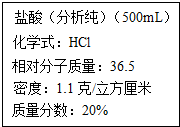 某学校实验室从化学试剂商店买回的一瓶未开封的盐酸试剂(氯化氢水溶液),试剂瓶的标签上的部分内容如图,请仔细阅读后计算
某学校实验室从化学试剂商店买回的一瓶未开封的盐酸试剂(氯化氢水溶液),试剂瓶的标签上的部分内容如图,请仔细阅读后计算