题目内容
13.下列推理结果正确的是( )| A. | 氧化物一定含有氧元素,所以含氧元素的物质一定是氧化物 | |
| B. | 化学反应前后原子种类不变,数目没有增减,所以化学反应一定遵循质量守恒定律 | |
| C. | 燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
分析 氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素;氧化物一定含有氧元素,所以含氧元素的物质一定是氧化物错误,如高锰酸钾不属于氧化物;化学反应前后原子种类不变,数目没有增减,所以化学反应一定遵循质量守恒定律正确;燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧错误,如电灯发光发热,但不是燃烧;碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐错误,如锌和盐酸反应也有气体放出.
解答 解:A、氧化物一定含有氧元素,所以含氧元素的物质一定是氧化物错误,如高锰酸钾不属于氧化物,故选项错误;
B、化学反应前后原子种类不变,数目没有增减,所以化学反应一定遵循质量守恒定律正确;故选项正确;
C、燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧错误,如电灯发光发热,但不是燃烧;故选项错误;
D、碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐错误,如锌和盐酸反应也有气体放出,故选项错误;
故选B
点评 本考点考查了物质的分类、质量守恒定律、酸的性质等,要加强记忆有关的知识点,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
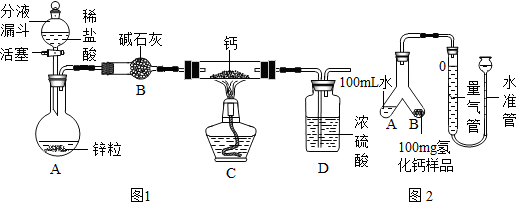
1.某课外活动小组的同学将16克氧化铜和过量的炭粉均匀混合,用如图1所示装置进行实验.图中铁架台等装置已略去.请回答有关问题:
(1)实验中最多能得到铜12.8克.

(2)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前.后测得的数据如下:
分析数据发现,反应中消耗碳和氧元素的质量大于(填“大于”或“小于”或“等于”生成二氧化碳的质量.下列4项中跟这一结果有关的有哪几项?AB.(填编号)
A.装置中还有一部分CO2未被NaOH溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(3)有同学认为用图2所示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2.N2和H2三种气体中,X应选择哪一种气体?N2.
(1)实验中最多能得到铜12.8克.

(2)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前.后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| A | 试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量54.8 克 |
| B | 反应后瓶内液体比反应前增重1.1 克 | |
A.装置中还有一部分CO2未被NaOH溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(3)有同学认为用图2所示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2.N2和H2三种气体中,X应选择哪一种气体?N2.
2.下列物质不属于金属材料的是( )
| A. | 青铜 | B. | 生铁 | C. | 赤铁矿 | D. | 钢 |