题目内容
1.某课外活动小组的同学将16克氧化铜和过量的炭粉均匀混合,用如图1所示装置进行实验.图中铁架台等装置已略去.请回答有关问题:(1)实验中最多能得到铜12.8克.

(2)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前.后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| A | 试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量54.8 克 |
| B | 反应后瓶内液体比反应前增重1.1 克 | |
A.装置中还有一部分CO2未被NaOH溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(3)有同学认为用图2所示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2.N2和H2三种气体中,X应选择哪一种气体?N2.
分析 (1)根据氧化铜的质量和化学方程式计算出铜的质量;
(2)通过数据处理,找出原因;
(3)考虑燃烧条件,分析可燃性的气体--氢气.
解答 解:(1)设实验中最多能得到铜的质量为x.
根据2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
160 128
16g x
列比例式为$\frac{160}{16g}=\frac{128}{x}$
x=12.8g,所以铜的质量为12.8克.故答案为12.8克;
(2)分析数据发现,反应中消耗碳和氧元素的质量:大于生成二氧化碳的质量;原因是:装置中还有一部分 CO2未被NaOH溶液吸收;氧化铜和炭粉反应产生的气体,除CO2外还有CO.答案合理即可.故填:大于;AB
(3)x应选择的气体是:N2(或氮气),故填:N2
点评 ①熟练掌握实验技能,②灵活运用质量守恒定律,根据化学方程式的计算③掌握碳的化学性质.

练习册系列答案
相关题目
12.物质的性质决定其用途.下列有关物质的用途说法错误的是( )
| A. | 石墨用于做电极 | B. | 稀有气体可用于焊接保护气 | ||
| C. | 农业上用食盐溶液选种 | D. | 氢氧化钠用于治疗胃酸过多 |
9.下列有关相对原子质量的叙述,错误的是( )
| A. | 相对原子质量没有单位 | |
| B. | 相对原子质量是以克为单位 | |
| C. | 相对原子质量就是一个原子的质量 | |
| D. | 相对原子质量只是一个比值,它的国际单位制(si)单位为一,符号为1(单位一般不写出) |
16.一定温度下,把10g某固体物质加入到100g水中,充分搅拌后发现还有部分固体未溶解,关于此时的溶液,下列说法正确的是( )
| A. | 它是浓溶液 | B. | 它是稀溶液 | ||
| C. | 它是不饱和溶液 | D. | 它是此温度下此溶质的饱和溶液 |
6.下列是一些实验基本操作的图示,请找出正确的( )
| A. |  检查装置气密性 | B. |  过滤 | C. |  给液体加热 | D. |  倾倒液体 |
13.下列推理结果正确的是( )
| A. | 氧化物一定含有氧元素,所以含氧元素的物质一定是氧化物 | |
| B. | 化学反应前后原子种类不变,数目没有增减,所以化学反应一定遵循质量守恒定律 | |
| C. | 燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
10.下列实验操作不正确的是( )
| A. | 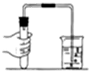 检查装置气密性 | B. | 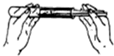 取用固体药品 | C. | 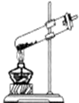 加热固体 | D. | 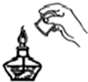 熄灭酒精灯 |
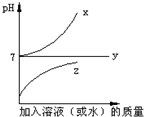 解释如图的函数图象
解释如图的函数图象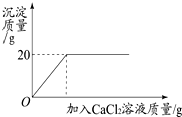 将一定质量的碳酸钠粉末溶于200g水中配制成溶液,向该溶液中加入20%的氯化钙溶液至不再产生白色沉淀,所得产生沉淀的质量与加入氯化钙溶液的质量关系如图所示,试计算:恰好完全反应不再产生白色沉淀时所用氯化钙溶液的质量.
将一定质量的碳酸钠粉末溶于200g水中配制成溶液,向该溶液中加入20%的氯化钙溶液至不再产生白色沉淀,所得产生沉淀的质量与加入氯化钙溶液的质量关系如图所示,试计算:恰好完全反应不再产生白色沉淀时所用氯化钙溶液的质量.