题目内容
3.过氧乙酸是一种常用的消毒剂,它的化学式为C2H4O3.试计算:(1)过氧乙酸分子中各原子的个数比为:2:4:3
(1)过氧乙酸中碳、氢、氧三种元素的质量比:6:1:12;
(2)过氧乙酸中所含的氢元素质量分数是多少?(要有计算步骤)
分析 (1)根据1个过氧乙酸分子的构成进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:(1)一个过氧乙酸分子是由2个碳原子、4个氢原子、3个氧原子构成的,故过氧乙酸分子中碳、氢、氧的原子个数比依次为2:4:3.
(2)过氧乙酸中碳、氢、氧元素的质量比为(12×2):(1×4):(16×3)=6:1:12.
(3)过氧乙酸中所含的氢元素质量分数是$\frac{12×2}{12×2+1×4+16×3}×$100%≈31.6%.
故答案为:(1)2:4:3;(2)6:1:12;(3)31.6%.
点评 本题难度不大,考查同学们灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
18.“雾霾”成为2014年两会最热词汇,雾霾治理已经成为热点话题.《环境空气质量标准》新增PM2.5指标,PM2.5是指直径小于或等于2.5um的颗粒物.为实现空气质量达标,合理的做法是( )
| A. | 煤炭直接燃烧 | B. | 秸秆焚烧还田 | ||
| C. | 开发清洁能源 | D. | 通过加高烟囱排放工业废气 |
8.制造太阳能电池需要高纯度的硅,工业上将含杂质的粗硅,制成高纯度硅常通过以下反应:①Si(固)+3HCl(气)$\frac{\underline{\;900℃\;}}{\;}$SiHCl3(气)+H2(气)+热量; ②SiHCl3+H2$\frac{\underline{\;950℃\;}}{\;}$Si+3HCl.上述两个反应都属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
15.溶液与我们的生活息息相关.下了有关溶液的说法正确的是( )
| A. | 配置5%的医用葡萄糖溶液的一般步骤是计算,称量和溶解 | |
| B. | 氢氧化钠溶液能导电是因为溶液中含有较多自由移动的离子 | |
| C. | 硝酸钾的饱和溶液通过降温可以变成硝酸钾的不饱和溶液 | |
| D. | 消除路面上的积雪可以撒些盐,这样可以使雪较快地融化 |
12.物质的性质决定其用途.下列有关物质的用途说法错误的是( )
| A. | 石墨用于做电极 | B. | 稀有气体可用于焊接保护气 | ||
| C. | 农业上用食盐溶液选种 | D. | 氢氧化钠用于治疗胃酸过多 |
13.下列推理结果正确的是( )
| A. | 氧化物一定含有氧元素,所以含氧元素的物质一定是氧化物 | |
| B. | 化学反应前后原子种类不变,数目没有增减,所以化学反应一定遵循质量守恒定律 | |
| C. | 燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
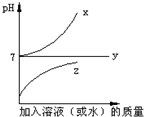 解释如图的函数图象
解释如图的函数图象