题目内容
3.在10℃时,将m克某物质溶于水后,得到溶质的质量分数为20%的饱和溶液,该饱和溶液中溶质、溶剂、溶液的质量比为1:4:5.分析 根据饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,进行分析解答.
解答 解:饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,得到溶质的质量分数为20%的饱和溶液,设该物质的溶解度为x,则
$\frac{x}{x+100g}×$100%=20% x=25g.
10℃时某物质的溶解度为36g,其涵义是10℃时,100g水中最多溶解25g某物质,溶液达到饱和状态,则该饱和溶液中溶质、溶剂、溶液的质量比为25g:100g:125g=1:4:5.
故答案为:1:4:5.
点评 本题难度不大,掌握饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%、溶解度的含义是正确解答本题的关键.

练习册系列答案
相关题目
11.盐酸和硫酸是常见的酸,某化学学习小组探究了它们的一些性质.
(1)用稀硫酸和盐酸均可以去除铁锈(主要成分为Fe2O3).某化学兴趣小组为探究哪种微粒能使氧化铁溶解,设计了如下实验方案,并得出初步结论.
①填写下表中的实验结论.
②同学们认为不需要做“向Fe2O3中加入水”的对比实验,其中的理由是什么?
(2)同学们把如图1甲、乙所示实验完成后,依次将废液缓慢倒入同一洁净的烧杯中.当倾倒液体时,观察到废液中有气泡产生.
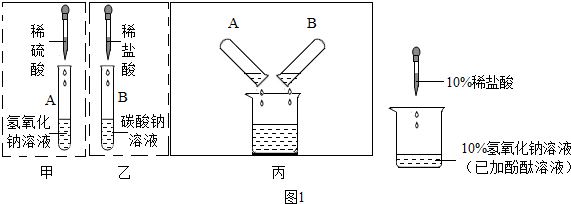
①经讨论确定,A试管中废液里的溶质是Na2SO4、H2SO4(写化学式,下同);B试管中废液里的溶质是NaCl、Na2CO3.
②在丙所示实验过程中有气体产生,请写出此反应的化学方程式.
(3)盐酸与氢氧化钠反应放热,如图2(左)所示为二者溶液混合的探究实验.随着盐酸的不断滴入,烧杯中溶液温度的变化如图2所示.
①b点时如图呈酸性(填“酸性”、“碱性”或“中性”).
②当溶液温度为38℃时,可证明溶液中氢氧化钠已经不存在的实验现象是什么?
(4)称取铜、锌混合物粉末10g置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时用去49g稀硫酸,且烧杯中剩余固体的质量为3.5g.请计算:所用的稀硫酸中溶质的质量分数是多少?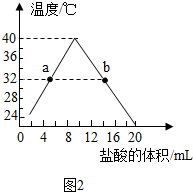
(1)用稀硫酸和盐酸均可以去除铁锈(主要成分为Fe2O3).某化学兴趣小组为探究哪种微粒能使氧化铁溶解,设计了如下实验方案,并得出初步结论.
①填写下表中的实验结论.
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有少量Fe2CO3的试管中分别加入NaCl溶液和Na2SO4溶液,振荡 | 固体不溶解 | ${SO}_{4}^{2-}$或Cl-不能使Fe2O3溶解;H2O分子不能使Fe2O3溶解 |
(2)同学们把如图1甲、乙所示实验完成后,依次将废液缓慢倒入同一洁净的烧杯中.当倾倒液体时,观察到废液中有气泡产生.

①经讨论确定,A试管中废液里的溶质是Na2SO4、H2SO4(写化学式,下同);B试管中废液里的溶质是NaCl、Na2CO3.
②在丙所示实验过程中有气体产生,请写出此反应的化学方程式.
(3)盐酸与氢氧化钠反应放热,如图2(左)所示为二者溶液混合的探究实验.随着盐酸的不断滴入,烧杯中溶液温度的变化如图2所示.
①b点时如图呈酸性(填“酸性”、“碱性”或“中性”).
②当溶液温度为38℃时,可证明溶液中氢氧化钠已经不存在的实验现象是什么?
(4)称取铜、锌混合物粉末10g置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时用去49g稀硫酸,且烧杯中剩余固体的质量为3.5g.请计算:所用的稀硫酸中溶质的质量分数是多少?

8.下列实验方案合理的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去二氧化碳中少量的一氧化碳 | 通入氧气、点燃 |
| B | 检验氧气和二氧化碳 | 加澄清石灰水 |
| C | 验证锌、铜、金的金属活动性 | 加盐酸 |
| D | 除去生石灰中少量的碳酸钙 | 加水充分搅拌 |
| A. | A | B. | B | C. | C | D. | D |
13.溶液与我们的生活息息相关,下列说法正确的是( )
| A. | 电解水时正极与负极产生的气体体积为2:1 | |
| B. | 衣服上的油污可利用洗涤剂的溶解或汽油乳化能将其洗去 | |
| C. | 溶液组成中不一定含有水 | |
| D. | 配制溶液时,只有搅拌或振荡才能加快物质的溶解速率 |

