题目内容
12.请根据如图的示的实验过程和提供的数据,计算下列问题.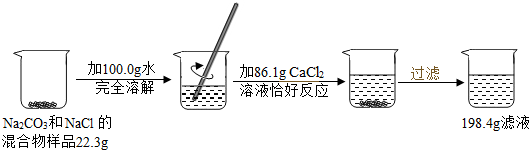
(1)反应后所得溶液中的溶质质量分数是多少?
(2)原混合物中的钠元素的质量分数是多少?
分析 (1)根据质量守恒定律可以知道,溶液减少的质量即为生成的碳酸钙的质量;根据碳酸钠和氯化钙反应的化学方程式结合碳酸钙的质量可以完成该题的解答;
(2)生成的氯化钠中的钠元素和原混合物中氯化钠所含钠元素的质量和混合物中钠元素的质量相等,所以可以据此结合钠元素的质量守恒来完成解答.
解答 解:(1)碳酸钙的质量=22.3g+100g+86.1g-198.4g=10g;
设纯碱样品中碳酸钠的质量为x,生成NaCl的质量为y
Na2CO3+CaCl2=2NaCl+CaCO3↓
106 117 100
x y 10g
$\frac{106}{x}=\frac{117}{y}=\frac{100}{10g}$
x=10.6g
y=11.7g
原有NaCl质量=22.3g-10.6g=11.7g
总共NaCl质量=11.7g+11.7g=23.4g
反应后所得溶液中的溶质质量分数是:$\frac{23.4g}{198.4g}×100%$=11.8%;
(2)根据反应前后元素的质量守恒,原混合物样品中钠元素的质量=23.4g×$\frac{23}{58.5}$=9.2g
原混合物中的钠元素的质量分数是:$\frac{9.2g}{22.3g}×100%$=41.3%
答:(1)反应后所得溶液中溶质的质量分数是11.8%;
(2)原混合物中的钠元素的质量分数是41.3%.
点评 本题中考查的知识点较多,主要是依据化学方程式进行计算,在解答时要注意运用质量守恒定律来得出计算所必须的已知量,然后依据化学方程式进行计算,同时要学会求算物质中元素的质量.

练习册系列答案
相关题目
20.近年来我国大部分地区尤其是中东部地区雾霾天气严重,大大影响了人们的生活,工业污染物和汽车尾气等是形成雾霾天气的主要元凶.下列做法不合理的是( )
| A. | 出门多乘坐公交车,少开私家车 | |
| B. | 为了减小PM2.5对环境的影响,停止冬季家庭供暖 | |
| C. | 推进汽车油品升级,减少有害物质排放 | |
| D. | 为了身体健康,少吸或不吸烟 |
17.酸溶液中都含有H+,因此不同的酸表现出一些共同的性质.下列关于稀H2SO4性质的描述中不属于酸的共同性质的是( )
| A. | 能和氢之前的金属反应放出氢气 | |
| B. | 能与石灰水反应生成盐和H2O | |
| C. | 能与BaCl2溶液反应生成BaSO4白色沉淀 | |
| D. | 能和碳酸盐反应冒出大量气泡 |
2.由于化学物质使用不当,给人印象不佳的化学名词越来越多:苏丹红、吊白块、三聚氰胺…下列做法不会危及人体健康的是( )
| A. | 用地沟油烹饪食物 | B. | 用甲醛水溶液浸泡鲜竹笋 | ||
| C. | 用小苏打作发酵粉焙制糕点 | D. | 向牛奶中添加三聚氰胺 |

 麻婆豆腐在清朝末年便被列为成都经典名菜.其配料见下表,此菜富含动植物蛋白质、钙、磷、铁、维生素及碳水化合物.具有温中益气、解毒润燥等功效.
麻婆豆腐在清朝末年便被列为成都经典名菜.其配料见下表,此菜富含动植物蛋白质、钙、磷、铁、维生素及碳水化合物.具有温中益气、解毒润燥等功效.