题目内容
3.某化学小组为测定一瓶失去标签的盐酸的溶质质量分数,实验设计如下:取纯净碳酸钙粉末5g于烧杯中,加入20g该盐酸溶液,充分反应后,过滤、洗涤、干燥,称量得剩余固体3g.
请利用上述数据计算该盐酸的溶质质量分数.(写出计算过程)
分析 剩余的3g固体为未反应的碳酸钙的质量,根据化学方程式和参加反应的碳酸钙的质量计算出氯化氢的质量,进而求质量分数.
解答 解:设参加反应的HCl质量为x
由题意分析可知,消耗碳酸钙质量为5g-3g=2g
2HCl+CaCO3═CaCl2+H2O+CO2↑
73 100
x 2g
$\frac{73}{x}$=$\frac{100}{2g}$
解得x=1.46 g
盐酸的溶质质量分数为:$\frac{1.46g}{20g}$×100%=7.3%
答:盐酸的溶质质量分数为7.3%.
点评 本题主要考查根据化学方程式的计算,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.如图为配制50g溶质质量分数为10%的氯化钠溶液的操作过程,下列有关操作与目的分析均正确的是( )


| 选项 | 操作 | 目的 |
| A | 用剩的食盐放回原试剂瓶 | 避免浪费 |
| B | 天平调平后在左、右托盘中各垫一张相同的纸 | 保证称取的食盐质量更准确 |
| C | 用50mL量筒替代天平量取所需的水 | 更加简便 |
| D | 溶解时用玻璃棒搅拌 | 增加食盐的溶解能力 |
| A. | A | B. | B | C. | C | D. | D |
7.央视二套《这是真的吗》栏目播出了电脑浸在溶液中也能正常工作的新鲜事.原来这种无色的液体是被称为“绝缘液”的液态一氟二氯乙烷.这种液体可为手机、电脑“洗澡”,用来清洗电子产品.一氟二氯乙烷的化学式为CCl2FCH3.下列对一氟二氯乙烷的认识,正确的是( )
| A. | 一氟二氯乙烷是无机物 | |
| B. | 一氟二氯乙烷由5种元素组成 | |
| C. | 一氟二氯乙烷的相对分子量为117克 | |
| D. | 一氟二氯乙烷中碳元素与氢元素的质量比为8:1 |
8.我市有些滩涂地区的土壤被称为“盐碱地“,当地农民常用引进内河淡水浸泡再排水的方法改良土壤.若以土壤pH为纵坐标,浸泡水次数(m)为横坐标,下列能正确表示土壤pH变化的图象的是( )
| A. | 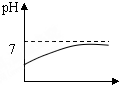 | B. | 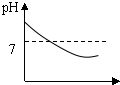 | C. |  | D. | 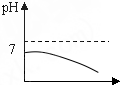 |
15.现有一白色粉末状物质X,为检验其成分,分别取三份少量固体放入试管中,进行如下实验,请根据实验现象判断,符合条件的物质X的化学式为( )
| 操作 | 滴加水 | 滴加稀硫酸 | 滴加硝酸钡溶液 |
| 现象 | 无色溶液 | 产生气体 | 产生白色沉淀 |
| A. | CuSO4 | B. | Na2CO3 | C. | Na2SO4 | D. | CaCO3 |

 小华在试管内进行了镁与盐酸反应的实验(如图).他观察到镁与盐酸剧烈反应,并伴有下列现象:(1)产生大量气泡;(2)试管壁发热;反应完毕,细心的小华还发现上部试管壁上出现了许多小水珠.请你解释其原因:反应放热,使水分蒸发到试管壁上,形成水珠.
小华在试管内进行了镁与盐酸反应的实验(如图).他观察到镁与盐酸剧烈反应,并伴有下列现象:(1)产生大量气泡;(2)试管壁发热;反应完毕,细心的小华还发现上部试管壁上出现了许多小水珠.请你解释其原因:反应放热,使水分蒸发到试管壁上,形成水珠.