题目内容
12.下列说法正确的是( )| A. | 硝酸铵溶于水时溶液温度升高 | |
| B. | 生活中为了降低水的硬度往往采用加热煮沸的方法 | |
| C. | 浓硫酸露置于空气中,溶质质量分数变大 | |
| D. | 为治理雾霾,禁止使用化石燃料 |
分析 A、硝酸铵溶于水吸热,溶液温度降低;B、根据硬水软化的方法考虑;C、根据浓硫酸的吸水性考虑;D、根据防治雾霾的方法考虑.
解答 解:A、硝酸铵溶于水吸热,溶液温度降低,故A错;
B、硬水软化的方法:加热煮沸和蒸馏,故B正确;
C、浓硫酸具有吸水性,溶质质量分数减小,故C错;
D、为治理雾霾,减少使用化石燃料,故D错.
故选B.
点评 解答本题关键是知道常见物质溶于水能量变化情况,知道硬水软化的方法,浓硫酸的吸水性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.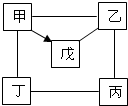 如图示中的“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下可以实现转化.下列四组选项中,符合图示要求的是( )
如图示中的“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下可以实现转化.下列四组选项中,符合图示要求的是( )
 如图示中的“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下可以实现转化.下列四组选项中,符合图示要求的是( )
如图示中的“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下可以实现转化.下列四组选项中,符合图示要求的是( )| 甲 | 乙 | 丙 | 丁 | 戊 | |
| A | Fe | H2SO4 | NaOH | CuCl2 | Fe2O3 |
| B | H2 | CuO | HCl | O2 | CO |
| C | H2SO4 | Fe2O3 | HCl | Zn | CuCl2 |
| D | Na2CO3 | Ca(OH)2 | NaOH | HCl | CO2 |
| A. | A | B. | B | C. | C | D. | D |
20.端午节是我国传统节日,我国民间有端午节用艾草辟邪的习俗,艾草中含有丰富的黄酮素(化学式为C15H10O2),有很高的药用价值.下列关于黄酮素的叙述错误的是( )
| A. | 黄酮素属于有机化合物 | |
| B. | 黄酮素中碳、氢元素的质量比为18:1 | |
| C. | 黄酮素的相对分子质量为222 | |
| D. | 黄酮素由27个原子构成 |
7.化学与生活密切相关,下列叙述中正确的是( )
| A. | 铁质刀具表面涂油可以防止生锈 | |
| B. | 为了个人卫生,应全部使用一次性的木筷和餐盒 | |
| C. | 人体缺锌会引起生长发育缓慢,因此锌元素摄入得越多越好 | |
| D. | 铵态氮肥与草木灰混合使用会降低肥效 |
17.下列关于金属和金属材料的说法不正确的是( )
| A. | 生铁和黄铜都能与稀硫酸反应 | |
| B. | 合金的硬度一般比组成它的纯金属的硬度大 | |
| C. | 铝的金属活动性比铁强,因此铝制品在空气中更易腐蚀 | |
| D. | 一氧化碳还原氧化铁过程中一氧化碳发生了氧化反应 |
1.下列说法正确的是( )
| A. | 蜡烛刚刚熄灭时产生的白烟是二氧化碳气体 | |
| B. | 氢氧化钠固体易潮解,可做某些气体的干燥剂 | |
| C. | 二氧化碳不供给呼吸,不宜作为植物的养料 | |
| D. | 大量使用化石燃料会造成大气污染,应该停止对化石燃料的开采和利用 |
 甲和乙两种固体物质的溶解度曲线如图所示,回答下列问题:
甲和乙两种固体物质的溶解度曲线如图所示,回答下列问题: