题目内容
10.食用碱的主要成分是Na2CO3(常含有少量的NaCl).某探究小组为测定市售食用碱中Na2CO3的含量,设计了如下实验装置.下列说法正确的是( )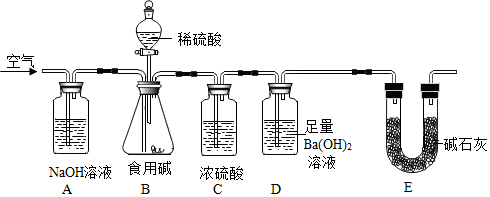
| A. | 装置A和E的作用相同 | |
| B. | 利用装置D的质量变化测定食用碱中Na2CO3的含量 | |
| C. | 若撤除装置A,直接通入空气会导致实验结果偏大 | |
| D. | 若撤除装置C,对实验结果的影响是偏小 |
分析 A、根据A中的氢氧化钠是吸收空气中的二氧化碳,E装置中的碱石灰也是吸收空气中的二氧化碳和水蒸气,防止对实验结果的干扰进行分析;
B、根据碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,二氧化碳和氢氧化钡反应生成碳酸钡沉淀和水,依据氢氧化钡增加的质量,可以计算碳酸钠的质量,但是没有样品的质量,不能计算食用碱中Na2CO3的含量进行分析;
C、根据空气中的二氧化碳会与氢氧化钠反应,如果撤掉A,会使空气中的二氧化碳未除导致实验结果偏大进行分析;
D、根据空气中的二氧化碳会与氢氧化钡反应,装置B中产生导出的气体中含有水,如果不除去气体中的水,会使D中测定的二氧化碳的质量增大进行分析.
解答 解:A、A中的氢氧化钠是吸收空气中的二氧化碳,E装置中的碱石灰是吸收空气中的二氧化碳和水蒸气,所以装置A和E的作用不相同,故A错误;
B、碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,二氧化碳和氢氧化钡反应生成碳酸钡沉淀和水,依据氢氧化钡增加的质量,可以计算碳酸钠的质量,但是没有样品的质量,不能计算食用碱中Na2CO3的含量,故B错误;
C、空气中的二氧化碳会与氢氧化钠反应,如果撤掉A,会使空气中的二氧化碳没有除去,导致实验结果偏大,故C正确;
D、空气中的二氧化碳会与氢氧化钡反应,装置B中产生导出的气体中含有水,如果不除去气体中的水,会使D中测定的二氧化碳的质量增大,故D错误.
故选:C.
点评 本题考查学生对实验原理及装置理解、对操作的评价、物质含量的测定、化学计算等,难度中等,根据物质的化学性质,要认真分析,把握实验设计的每个步骤中的实验目的.

练习册系列答案
相关题目
20.归纳是一种重要的学习方法.下列归纳中错误的是( )
| A. | 酸都能与盐发生复分解反应 | B. | 氧化物都只有两种元素 | ||
| C. | 所有化学变化都遵守质量守恒定律 | D. | 物质与氧气的反应都属于氧化反应 |
18.由A、B两种元素组成的化合物中A、B的质量比为3:1,A与B的相对原子质量比为12:1,则该化合物化学式为( )
| A. | AB | B. | AB2 | C. | AB4 | D. | A2B |
15.从化学角度分析,下列诗句只涉及物理变化的是( )
| A. | 炉火照天地,红星乱紫烟 | B. | 夜来风雨声,花落知多少 | ||
| C. | 粉身碎骨浑不怕,要留清白在人间 | D. | 月落乌啼霜满天,江枫渔火对愁眠 |
2.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,滤液仍为蓝色,滤渣中所含物质不可能的情况是( )
| A. | .可能有银和铜,没有锌 | B. | .可能只有银,没有铜和锌 | ||
| C. | 一定有银,可能有铜和锌 | D. | .一定有银、没有锌,可能有铜 |
20.下列物质中,属于纯净物的是( )
| A. | 纯净的盐酸 | B. | 生理盐水 | C. | 洁净的空气 | D. | 冰水混合体 |
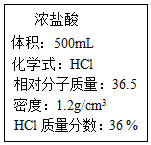 某浓盐酸瓶上的标签如图所示.求:
某浓盐酸瓶上的标签如图所示.求: