题目内容
5.医疗上颇为流行的“理疗特热法”就是利用铁粉缓慢氧化放出的热均匀稳定,使病员患处保持温热活血状态.则5.6g铁粉完全氧化成红色粉末Fe2O3,消耗氧气的质量为2.4克,其化学方程式为4Fe+3O2=2Fe2O3;实验室中可用加热高锰酸钾的方式制氧气,其化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.分析 铁和氧气发生缓慢氧化生成氧化铁,根据反应的化学方程式及其铁粉质量可以计算反应需要氧气的质量;
高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气.
解答 解:设消耗氧气的质量为x,
4Fe+3O2=2Fe2O3,
224 96
5.6g x
$\frac{224}{5.6g}$=$\frac{96}{x}$,
x=2.4g,
高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
故填:2.4;4Fe+3O2=2Fe2O3;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
15.安全、健康是永恒的话题,下列做法符合安全健康规范的是( )
| A. | 进入地下煤矿前先做灯火实验 | |
| B. | 尽量多地食用红肉补铁 | |
| C. | 用甲醛漂洗牛血旺 | |
| D. | 天然气泄漏立即关闭闸阀并开窗通风 |
10.食用碱的主要成分是Na2CO3(常含有少量的NaCl).某探究小组为测定市售食用碱中Na2CO3的含量,设计了如下实验装置.下列说法正确的是( )
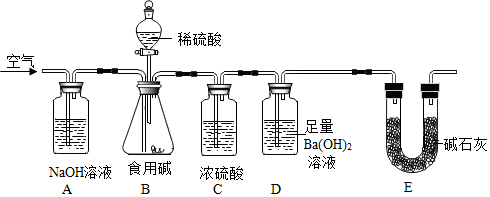

| A. | 装置A和E的作用相同 | |
| B. | 利用装置D的质量变化测定食用碱中Na2CO3的含量 | |
| C. | 若撤除装置A,直接通入空气会导致实验结果偏大 | |
| D. | 若撤除装置C,对实验结果的影响是偏小 |
17.以下事实用微观粒子的知识解释错误的是( )
| 选项 | 事实 | 解释 |
| A | 一畦春韭绿,十里稻花香 | 分子不断运动 |
| B | 水结冰后体积变大 | 水分子体积变大 |
| C | 1滴水中大约有1.67×1021个水分子 | 分子很小 |
| D | 6000L氧气加压后可装入容积为40L的钢瓶中 | 分子间有间隔 |
| A. | A | B. | B | C. | C | D. | D |
14.下列各组物质的分离操作可按溶解、过滤、蒸发溶剂的顺序进行的是( )
| A. | 食盐和蔗糖 | B. | 铜粉和铁粉 | ||
| C. | 水和酒精的混合物 | D. | 食盐和泥沙 |
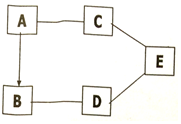 A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去),请回答下列问题:
A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去),请回答下列问题: