题目内容
9.在Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,则滤出的固体中一定含有铜、铁,上述过程中所发生有关反应的化学方程式为Fe+Cu(NO3)2═Fe(NO3)2+Cu(或Fe+2HCl═FeCl2+H2↑)(写出一个即可)分析 在Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的铁粉,铁的金属活动性比铜强,比锌弱,能与Cu(NO3)2溶液反应生成硝酸亚铁溶液和铜,不能与硝酸锌反应;充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,说明有能与稀硫酸反应的金属存在,即铁有剩余,据此进行分析解答.
解答 解:在Cu(NO3)2和Zn(NO3)2的混合溶液中加入一定量的铁粉,铁的金属活动性比铜强,比锌弱,能与Cu(NO3)2溶液反应生成硝酸亚铁溶液和铜,不能与硝酸锌反应;充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,说明有能与稀硫酸反应的金属存在,即铁有剩余,则滤出的固体中一定含有铜、铁.
铁与Cu(NO3)2溶液反应生成硝酸亚铁溶液和铜,反应的化学方程式为Fe+Cu(NO3)2═Fe(NO3)2+Cu;铁与稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:铜、铁;Fe+Cu(NO3)2═Fe(NO3)2+Cu(或Fe+2HCl═FeCl2+H2↑).
点评 本题难度不大,掌握金属的化学性质、由滤出的固体中滴加稀硫酸有气泡产生确定滤出的固体的成分是正确解答本题的关键.

练习册系列答案
相关题目
19.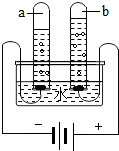 小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )
小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )
 小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )
小左做完电解水后的装置情况如图所示.关于本次实验,以下说法不正确的是( )| A. | a试管中收集到的气体是氢气 | |
| B. | 可以用带火星的木条检验b试管中收集的气体 | |
| C. | a、b两支试管中所收集气体的质量比为2:1 | |
| D. | 该实验可以证明水中含有氢氧两种元素 |
17.下列物质的化学式、俗名和类别全部正确的是( )
| A. | 烧碱 Na2CO3 盐 | B. | 酒精 C2H5OH 氧化物 | ||
| C. | 熟石灰 Ca(OH)2 碱 | D. | 盐酸 NaCl 酸 |
4.根据化学方程式Cl2+SO2+2H2O═H2SO4+2X可推断X的化学式是( )
| A. | SO3 | B. | H2 | C. | HCl | D. | S |
14.下列物质的俗称(或主要成分)与化学式不对应的是( )
| A. | 干冰--CO2 | B. | 大理石--CaCO3 | C. | 沼气--CH4 | D. | 熟石灰--CaO |
1.现有三瓶标签已经损坏的无色溶液:稀硫酸、氯化钠、硝酸银,如果请你来帮他们一次鉴别出来,你会选择哪种药品( )
| A. | 无色酚酞 | B. | 氢氧化钠溶液 | C. | 铁钉 | D. | 紫色石蕊 |