题目内容
19.在硬质玻璃管里内放入4.5g氧化铜粉末,用一氧化碳还原它,在停止加热冷却后,称得硬质玻璃管里的固体粉末为4g,求有几克氧化铜被还原?分析 根据固体的质量差,利用化学反应方程式来计算反应的一氧化碳的质量,进一步确定剩余固体的成分,及它们的质量.
解答 解:设参加反应的氧化铜的质量为x,则.
CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 △m
80 64 80-64=16
x 4.5g-4g=0.5g
$\frac{80}{x}$=$\frac{16}{0.5g}$,
解得x=2.5g,
答:有2.5g氧化铜被还原.
点评 本题考查学生利用差量法和化学反应方程式的计算,学生应明确该反应中固体不一定完全反应,不可将混合物质量直接代入化学方程式计算.

练习册系列答案
相关题目
10.除去下列物质中混有的少量杂质,所用试剂和操作方法均正确的是( )
| 序号 | 物质 | 杂质 | 所用试剂和操作方法 |
| A | CO2 | HCl | 通过足量的NaOH溶液,再通过浓硫酸干燥 |
| B | NaNO3溶液 | Na2SO4 | 加入过量的Ba(OH)2溶液,过滤 |
| C | NaCl固体 | 细沙 | 加入足量水溶解,过滤 |
| D | 铜粉 | 铁粉 | 加入适量的稀盐酸,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
14.某白色固体可能由CaCO3、NaCl、BaCl2 NaOH Na2SO4中的一种或几种组成的,实验记录如图:下列分析正确的是( )
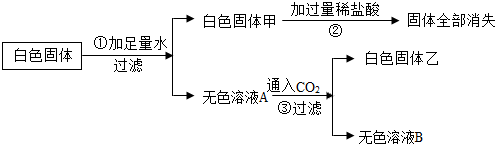

| A. | 原固体中不含BaCl2、Na2SO4 | |
| B. | 原固体中一定含有CaCO3、BaCl2、NaOH | |
| C. | 步骤②中得到的溶液中溶质是CaCl2 | |
| D. | 确定固体中是否有NaCl可以取无色溶液A直接滴入AgNO3溶液 |
4.我市的许多超市定期使用“84消毒液”进行消毒杀菌,该消毒液的主要成分是次氯酸钠、化学式为NaClO.关于次氯酸钠,以下说法正确的是( )
| A. | NaClO是一种氧化物 | |
| B. | NaClO中氯元素的质量分数最大 | |
| C. | NaClO中氯元素的化合价为-1价 | |
| D. | NaClO中Na、Cl、O三种元素的质量比1:1:1 |
