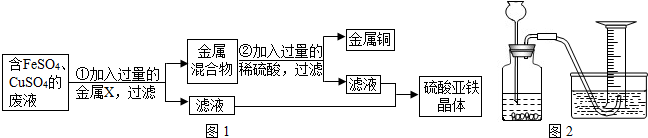
题目内容
 以下五种为初中常见物质,均由表中元素组成
以下五种为初中常见物质,均由表中元素组成 | 元素名称 | 氢 | 碳 | 氧 | 氯 | 钙 | 铁 |
| 元素符号 | H | C | O | Cl | Ca | Fe |
(2)若甲、乙均为氧化物、乙为红色固体,则甲、乙发生反应的化学方程式为
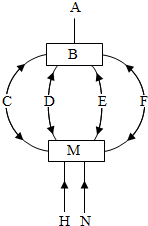
(3)如图为九种物质的相互关系,其中A、B、M、N是氧化物,C、H是单质,只有D、E中含有三种元素,D能使紫色石蕊溶液变成红色,图中“→”表示转关系“-”表示反应关系(部分物质和反应条件为标出)则:D的化学式为
考点:物质的鉴别、推断,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:常见物质的推断题
分析:(1)根据铁在氧气中燃烧的现象考虑;
(2)考虑氧化铁的颜色;
(3)根据题意:“A、B、M、N是氧化物,C、H是单质,只有D、E中含有三种元素,D能使紫色石蕊溶液变成红色”,特别是“D、E中含有三种元素,D能使紫色石蕊变红色”,可推测出各物质.代入验证,是否符合.
(2)考虑氧化铁的颜色;
(3)根据题意:“A、B、M、N是氧化物,C、H是单质,只有D、E中含有三种元素,D能使紫色石蕊溶液变成红色”,特别是“D、E中含有三种元素,D能使紫色石蕊变红色”,可推测出各物质.代入验证,是否符合.
解答:解:(1)铁在氧气中燃烧的现象是:剧烈燃烧、火星四射、生成黑色固体放出热量,由甲在乙中燃烧,火星四射,生成黑色固体,可知是铁在氧气中燃烧,生成物是四氧化三铁;
(2)若甲、乙均为氧化物、乙为红色固体,则甲、乙发生反应,即一氧化碳与氧化铁在高温下反应生成二氧化碳和铁,其反应的化学方程式为:3CO+Fe2O3
2Fe+3CO2,.
(3)根据题目的突破口:“A、B、M、N是氧化物,C、H是单质,只有D、E中含有三种元素,D能使紫色石蕊溶液变成红色”,则可推测出“D能使紫色石蕊变红色”为碳酸,其化学式是:H2CO3;则:A为氧化钙,B为水,C为氧气,H为碳,D为碳酸,E为碳酸钙,F为HCl或CH4,N为一氧化碳.代入验证,符合题意.
A与B反应为氧化钙与水的反应生成氢氧化钙,化学方程式:CaO+H2O═Ca(OH)2;反应符合“多变一”的特点,故基本反应类型是:化合反应.
故答案为:
(1)Fe3O4.
(2)3CO+Fe2O3
2Fe+3CO2.
(3)H2CO3. CaO+H2O═Ca(OH)2. 化合,HCl或CH4.
(2)若甲、乙均为氧化物、乙为红色固体,则甲、乙发生反应,即一氧化碳与氧化铁在高温下反应生成二氧化碳和铁,其反应的化学方程式为:3CO+Fe2O3
| ||
(3)根据题目的突破口:“A、B、M、N是氧化物,C、H是单质,只有D、E中含有三种元素,D能使紫色石蕊溶液变成红色”,则可推测出“D能使紫色石蕊变红色”为碳酸,其化学式是:H2CO3;则:A为氧化钙,B为水,C为氧气,H为碳,D为碳酸,E为碳酸钙,F为HCl或CH4,N为一氧化碳.代入验证,符合题意.
A与B反应为氧化钙与水的反应生成氢氧化钙,化学方程式:CaO+H2O═Ca(OH)2;反应符合“多变一”的特点,故基本反应类型是:化合反应.
故答案为:
(1)Fe3O4.
(2)3CO+Fe2O3
| ||
(3)H2CO3. CaO+H2O═Ca(OH)2. 化合,HCl或CH4.
点评:解答本题关键是要知道铁在氧气中燃烧的现象等,解答本题还要注意利用所给的元素写化学式.且解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征及结构特征),导出结论,最后别忘了把结论代入原题中验证,若“路”走得通则已经成功.

练习册系列答案
相关题目
图示实验所得出的结论中,不正确的是( )
A、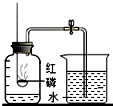 氧气约占空气体积的
| ||
B、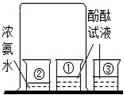 证明分子是不断运动的 | ||
C、 天平不平衡说明该反应不遵守质量守恒定律 | ||
D、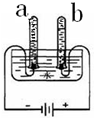 氢气与氧气的体积比为2:1 |
下列4个坐标图分别表示4个实验过程中某些质量的变化,其中正确的是( )
A、 向一定量石灰石中滴加稀盐酸 |
B、 向一定量的过氧化氯溶液中加入少量二氧化锰 |
C、 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 |
D、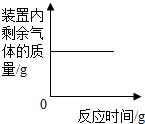 在某一密闭容器内点燃红磷 |
属于浊液的是( )
| A、香水 | B、“雪碧”汽水 |
| C、碘酒 | D、牛奶 |