题目内容
7. 为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:
为测定某氮肥中氮元素的质量分数是否与标签说明相符,小玲取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液恰好反应,(杂质成分不含有氮元素,能溶于水但不参加反应)记录有关数据如表:请通过计算回答:| 反 应 前 | 反 应 后 | |
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液质量(滤液的损失忽略不计) |
| 45g | 85g | 106.7g |
(2)反应前后,溶液中硫元素的质量是减小(填“不变”、“增大”或“减小”).
(3)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中氮元素的含量是否与标签相符.(请写出计算过程)
分析 (1)根据反应前后物质的总质量相等即可求出生成的硫酸钡沉淀的质量;
(2)根据氯化钡和硫酸铵反应生成硫酸钡沉淀和氯化铵进行分析;
(3)根据沉淀的质量可以求出参加反应的硫酸铵的质量,进一步计算氮肥中氮元素的含量.
解答 解:(1)依据质量守恒定律可知,反应生成硫酸钡沉淀的质量为:45g+85g-106.7g=23.3g;
(2)氯化钡和硫酸铵反应生成硫酸钡沉淀和氯化铵,所以反应前后,溶液中硫元素的质量是减小;
(3)设硫酸铵的质量为x,
(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl
132 233
x 23.3g
$\frac{132}{x}$=$\frac{233}{23.3g}$
x=13.2g
13.2g硫酸铵中氮元素的质量13.2g×$\frac{2×14}{2×18+32+64}$×100%=2.8g
氮肥中氮元素的含量:$\frac{2.8g}{15g}$×100%=18.7%<20%,
所以不符合标准.
故答案为:(1)23.3;
(2)减小;
(3)不符合标准.
点评 本题考查的是根据化学方程式的计算,解答本题的关键是计算出生成的硫酸钡的质量,然后根据方程式计算即可.

练习册系列答案
相关题目
17.已知碳酸氢钠受热分解:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.现取Na2CO3和NaHCO3的混合物100g,加热到质量不再改变,剩余固体为69g.下列说法正确的是( )
| A. | 反应后生成CO2的质量为31 g | |
| B. | 原混合物中Na2CO3的质量分数为84% | |
| C. | 原混合物中NaHCO3的质量为42 g | |
| D. | 反应后生成CO2和H2O的质量比为22:9 |
12.下列对一些事实的解释不正确的是( )
| A. | 金刚石比石墨硬度大--碳原子的排列方式 | |
| B. | H2O2能杀菌消毒而H2O则不能--两种物质的分子构成不同 | |
| C. | 在草坪上滚动的足球,滚动的越来越慢--由于它的惯性越来越小 | |
| D. | 推土机上安装两条宽大的履带--是为了减小压强 |
19.豆浆被称为“植物奶“.其中含有的异黄酮(C15H10O2)其有防癌功能.下列有关异黄酮的说法正确的是( )
| A. | 异黄酮中碳元素的质量分数最大 | |
| B. | 异黄酮中C、H、O三种元素的质量比为15:10:2 | |
| C. | 异黄酮由15个碳原子、10个氢原子和2个氧原子构成 | |
| D. | 异黄酮属于氧化物 |
16.下列物质的用途中能体现出物质的化学性质的是( )
| A. | 空气液化分离氧气 | B. | 活性炭吸附色素异味 | ||
| C. | 铁制品表面镀金属 | D. | 汉白玉雕刻子路雕像 |


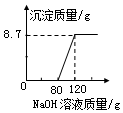 向盛有100g稀硫酸的烧杯中加入一定质量的镁粉,固体完全反应后,再向所得溶液中加入NaOH溶 液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示.请计算:
向盛有100g稀硫酸的烧杯中加入一定质量的镁粉,固体完全反应后,再向所得溶液中加入NaOH溶 液,所得沉淀的质量与加入NaOH溶液的质量关系如图所示.请计算: 如图是测定空气中氧气含量的实验装置图.实验如下:用注射器抽取30mL空气(活塞拉至30mL刻度处),硬质玻璃管中空气的体积为50mL;在硬质玻璃管中放入过量铜粉,在右侧导管口套上瘪的气球;点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL.
如图是测定空气中氧气含量的实验装置图.实验如下:用注射器抽取30mL空气(活塞拉至30mL刻度处),硬质玻璃管中空气的体积为50mL;在硬质玻璃管中放入过量铜粉,在右侧导管口套上瘪的气球;点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL.