题目内容
16.将无色液体A与黑色粉末B混合,能产生一种无色无味的气体C,C也是空气中的一种重要成分.若将淡黄色粉末D放入C中燃烧,火 焰呈蓝紫色,生成一种刺激气味的气体E,推断并写出上述各种物质的化学式.(1)AH2O2、BMnO2、CO2、DS、ESO2
(2)请写出相关化学方程式(或文字表达式):
①A与B 混合反应得到C:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②D与C反应:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
分析 根据C是空气中的一种重要成分,将淡黄色粉末D放入C中燃烧,火焰呈蓝紫色,生成一种刺激气味的气体E,所以C有助燃性,C是氧气,结合常见可燃物燃烧的现象可知,硫和氧气反应火焰呈蓝紫色,生成有刺激气味的二氧化硫,所以D是硫,E是二氧化硫,将无色液体A与黑色粉末B混合,能产生无色无味的气体---氧气C,结合实验室制取氧气的药品和方法可知,A是过氧化氢溶液,B是二氧化锰,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1)根据C是空气中的一种重要成分,将淡黄色粉末D放入C中燃烧,火焰呈蓝紫色,生成一种刺激气味的气体E,所以C有助燃性,C是氧气,结合常见可燃物燃烧的现象可知,硫和氧气反应火焰呈蓝紫色,生成有刺激气味的二氧化硫,所以D是硫,E是二氧化硫,将无色液体A与黑色粉末B混合,能产生无色无味的气体---氧气C,结合实验室制取氧气的药品和方法可知,A是过氧化氢溶液,B是二氧化锰,经过验证,推出的各种物质均满足题中的转化关系,推导正确,所以A是H2O2,B是MnO2,C是O2,D是S,E是SO2;
(2)①根据分析,A是H2O2,B是MnO2,C是O2,故A与B混合反应得到C,即过氧化氢在二氧化锰的催化作用下反应生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
②根据分析,C是O2,D是S,D与C反应,即硫和氧气在点燃的条件下生成二氧化硫,化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
故答案为:
(1)H2O2、MnO2、O2、S、SO2
(2)①2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.②S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

(1)表中磷元素属于非金属(填金属或非金属)元素.
(2)表中具有相对稳定结构的元素是Ar.(填元素符号)
(3)表中与氧原子具有相同化学性质的是硫(填元素名称).
| 元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
| 原子结构示意图 | 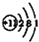 | 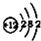 | 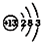 | 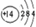 | 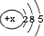 | 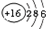 | 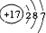 | 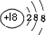 |
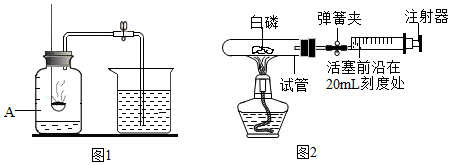
 研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.请根据图示实验回答下列问题.
研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.请根据图示实验回答下列问题.