题目内容
5.空气是一种宝贵的资源.(1)二百多年前,法国化学家拉瓦锡用定量的方法研究了空气的成分(装置如图).下列有关该实验的说法中,不正确的是C(填字母).
A.汞槽中的汞起到液封的作用
B.能将密闭装置内空气中的氧气几乎耗尽
C.银白色的液态汞剧烈燃烧,迅速变成红色粉末
D.生成的红色粉末加强热又能得到汞和氧气
(2)空气中的二氧化碳能产生温室效应.正是因为有了这种效应,全球平均地表温度才提高到目前适合人类生存的15℃.
(3)煤燃烧时排放出SO2、NO2(填化学式)等污染物.这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨.
(4)在汽油中加入适量C2H5OH(填化学式)作为汽车燃料,可适当节省石油资源,并在一定程度上减少汽车尾气的污染.
(5)利用空气制取氮肥的流程如图2所示:
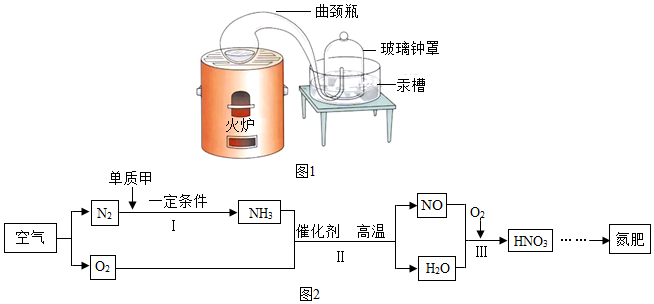
①Ⅰ中参加反应的单质甲是氢气.
②Ⅱ中发生反应的化学方程式是4NH3+5O2$\frac{\underline{\;催化剂\;}}{高温}$4NO+6H2O.
③物质所含元素化合价发生变化的反应都是氧化还原反应.因此,反应Ⅲ属于(填“属于”或“不属于”)氧化还原反应.
分析 (1)根据拉瓦锡实验的特点进行分析解答;
(2)根据温室效应的利弊解答.
(3)根据煤燃烧时排放出二氧化硫、二氧化氮等污染物进行解答;
(4)根据乙醇汽油的使用分析;
(5)①根据图示可知:Ⅰ中参加反应的单质甲为氢气解答;
②根据反应原理找出反应物、生成物、反应条件,写出反应的化学方程式解答;
③根据反应中所含元素化合价进行解答;
解答 解:(1)教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有在汞槽中起到液封作用;生成的化合物加热分解又能得到汞和氧气;能将密闭装置内空气中的氧气集合耗尽,但是汞不能燃烧,故选C;
(2)空气中的二氧化碳能产生温室效应,它使全球平均地表温度提高到目前适合人类生存的15℃.
(3)煤燃烧时排放出二氧化硫、二氧化氮等污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水会形成酸雨;
(4)乙醇具有可燃性可在汽油中加入适量作为汽车燃料;
(5)①氮气和氢气在一定条件下生成氨气,①Ⅰ中参加反应的单质甲为氢气;
②Ⅱ中反应的化学方程式为:4NH3+5O2$\frac{\underline{\;催化剂\;}}{高温}$4NO+6H2O;
③氮元素反应前化合价为+2价,反应后化合价为+5价,氧元素反应前化合价为0价,反应后化合价为-2价,反应Ⅲ属于氧化还原反应.
故答案为:(1)C;(2)温室;(3)SO2、NO2;(4)C2H5OH;(5)①氢气(或H2); ②4NH3+5O2$\frac{\underline{\;催化剂\;}}{高温}$4NO+6H2O;③属于.
点评 本题主要考查了空气组成的测定及对实验数据的分析,比较综合,要细心分析.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
16.下列对化学用语的表述正确的是( )
| A. | 2O-表示两个氧元素 | B. | N2-表示两个氮原子 | ||
| C. | Ca2+-表示钙元素显+2 | D. | 2H2O-表示2个水分子 |
13.M是生活中常用的金属,MSO4溶液是无色液,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是M>Al>Cu.
【实验探究】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因,该原因是铝表面有一层氧化膜.
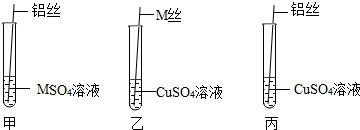
【继续探究】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
(1)试管乙中观察到的现象是M表面出现一层红色物质.
(2)试管丙中反应的化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu.
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管丙(填试管编号)中的实验,也可以得出正确的结论.
【得出结论】通过以上实验,同学们得出了三种金属的活动性顺序.
【反思与归纳】由上述实验得出比较金属活动性顺序的方法有:①金属和酸反应比较;②与氧气反应的剧烈程度.

【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是M>Al>Cu.
【实验探究】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
| 实验操作 | M丝插入试管①中 | 钢丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu:M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
【继续探究】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
(1)试管乙中观察到的现象是M表面出现一层红色物质.
(2)试管丙中反应的化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu.
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管丙(填试管编号)中的实验,也可以得出正确的结论.
【得出结论】通过以上实验,同学们得出了三种金属的活动性顺序.
【反思与归纳】由上述实验得出比较金属活动性顺序的方法有:①金属和酸反应比较;②与氧气反应的剧烈程度.
20.在校园科技节上,为测出鸡蛋壳(主要成分是碳酸钙)中钙元素的质量分数,某同学称取已洗净、晾干、研成粉末的鸡蛋壳10克置于烧杯中,将烧杯放在电子天平上,往烧杯中加入的稀盐酸,总重110g,每0.5分钟记录一次电子天平的示数,据此计算出产生气体的质量,具体数据如表:
(1)若产生的气体全部是鸡蛋壳中的碳酸钙与盐酸反应生成的CO2,根据实验结果计算出该鸡蛋壳中钙元素的质量分数.(假定鸡蛋壳中其它成分不含钙元素,写出具体计算过程)
(2)下列哪些情况会导致实验中钙元素质量分数测量结果偏大?C.
A.鸡蛋壳未晾干 B.鸡蛋壳未充分研碎 C.鸡蛋壳中含有碳酸镁(可与盐酸反应生成MgCl2、H2O和CO2)
| 时间(分钟) | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| 电子天平示数(克) | 110 | 108.2 | 107 | 106.4 | 106.4 | 106.4 | 106.4 |
(2)下列哪些情况会导致实验中钙元素质量分数测量结果偏大?C.
A.鸡蛋壳未晾干 B.鸡蛋壳未充分研碎 C.鸡蛋壳中含有碳酸镁(可与盐酸反应生成MgCl2、H2O和CO2)
17.正确反映对应变化关系的图象是( )
| A. |  向一定质量的水中加入硝酸钾晶体 | |
| B. |  向一定量的氧化铜中通入一氧化碳气体并加热 | |
| C. |  一定量的镁在空气中燃烧 | |
| D. |  在盛有空气的密闭容器中点燃红磷 |
15.下列关于铝等金属材料的说法,不正确的是( )
| A. | 铝是地壳中含量最多的元素 | |
| B. | 金属一般具有导电性、导热性和延展性 | |
| C. | 铝在空气中能生成一层致密的氧化物保护膜 | |
| D. | 保护金属资源的一条途径是禁止开采金属矿物质 |
 空气、水是人类赖以生存的自然资源.
空气、水是人类赖以生存的自然资源. 为了验证金属活动性强弱,同学们设计了如图所示的实验.
为了验证金属活动性强弱,同学们设计了如图所示的实验.