题目内容
20.在校园科技节上,为测出鸡蛋壳(主要成分是碳酸钙)中钙元素的质量分数,某同学称取已洗净、晾干、研成粉末的鸡蛋壳10克置于烧杯中,将烧杯放在电子天平上,往烧杯中加入的稀盐酸,总重110g,每0.5分钟记录一次电子天平的示数,据此计算出产生气体的质量,具体数据如表:| 时间(分钟) | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| 电子天平示数(克) | 110 | 108.2 | 107 | 106.4 | 106.4 | 106.4 | 106.4 |
(2)下列哪些情况会导致实验中钙元素质量分数测量结果偏大?C.
A.鸡蛋壳未晾干 B.鸡蛋壳未充分研碎 C.鸡蛋壳中含有碳酸镁(可与盐酸反应生成MgCl2、H2O和CO2)
分析 (1)根据质量守恒定律和碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,可知,反应中的质量减少量为生成的二氧化碳的质量.根据二氧化碳的质量对应出钙元素的质量,最后求算出钙元素在混合物中的质量分数.
(2)钙元素在混合物中的质量分数计算是$\frac{钙元素的质量}{鸡蛋壳的质量}×100%$,根据这个计算式子分析可能引起偏高的操作
解答 解:
(1)根据质量守恒定律可得,生成的二氧化碳的质量110g-106.4g=3.6g
设钙元素的质量为x.
根据CaCO3+2HCl=CaCl2+H2O+CO2↑
可得Ca~~CO2↑
40 44
x 3.6g
$\frac{40}{44}$=$\frac{x}{3.6g}$
x≈3.27g
则鸡蛋壳中钙元素的质量分数为$\frac{3.27g}{10g}$×100=32.7%
(2)由于钙元素在混合物中的质量分数计算是$\frac{钙元素的质量}{鸡蛋壳的质量}×100%$,当结果偏大时,要么是钙元素的质量偏大,要么鸡蛋壳的质量偏小.鸡蛋壳未晾干,会导致总质量相对于干燥鸡蛋壳偏大,所以引起的钙元素的质量分数偏小.而鸡蛋壳没有完全反应,则对应的二氧化碳偏少,则对应的钙元素质量也偏小,所以质量分数偏小.
而含有杂质碳酸镁时,消耗等质量的碳酸盐时,碳酸镁生成的二氧化碳多,而这个二氧化碳当成碳酸钙生成的,则对应的钙元素的质量就偏大,最终的钙元素的质量分数偏大.
故选:C.
点评 误差分析要结合计算公式分析,结合实验原理进行综合考虑.在根据方程式计算时,如果对应到元素的质量,则可以进一步转化为关系式法,减少计算过程的复杂.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
19.在密闭容器中,将一定质量的碳放在一定质量的氧气中燃烧,实验数据如下表,其中,实验数据无误的是( )
| 序号 | ① | ② | ③ |
| 氧气质量/g | 8 | 16 | 24 |
| 碳质量/g | 3 | 12 | 6 |
| 生成CO2质量/g | 11 | 22 | 22 |
| A. | ① | B. | ② | C. | ③ | D. | ①②③ |
15.下列各物质按单质、氧化物、混合物的顺序排列的是( )
| A. | 铁、氯酸钾、稀有气体 | B. | 二氧化碳、氮气、生理盐水 | ||
| C. | 臭氧、过氧化氢、可乐 | D. | 水、四氧化三铁、加碘食盐 |
10.保护环境,节约资源,从我做起,下列做法符合这一理念的是( )
| A. | 城市道路使用太阳能景观灯 | B. | 农田中的秸秆就地焚烧 | ||
| C. | 生活污水直接排放到河流中 | D. | 废旧电池掩埋在土壤中 |
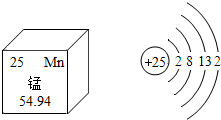 锰(Mn)是维持人体正常生命活动所必须的微量元素,含锰化合物在生产、生活中也被广泛应用.结合图中信息,回答下列问题.
锰(Mn)是维持人体正常生命活动所必须的微量元素,含锰化合物在生产、生活中也被广泛应用.结合图中信息,回答下列问题.