题目内容
15.如图是实验室制备物质的常用装置,根据装置回答:
(1)图中仪器m的名称为长颈漏斗,请写出用装置A制取一种气体的化学方程式为Zn+H2SO4=ZnSO4+H2↑,该反应的基本反应类型为置换反应.
(2)装置C可用于收集的常见气体是(写出一种即可)O2或CO2.
(3)若用装置B除去二氧化碳中少量的水蒸气,可在装置中装入浓硫酸,气体应从a端进入.
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;二氧化碳可以用浓硫酸干燥,干燥时要长进短出.
解答 解:(1)长颈漏斗方便加液体药品,实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;如果用双氧水和二氧化锰制氧气就不需要加热,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:长颈漏斗;Zn+H2SO4=ZnSO4+H2↑;置换反应(或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分解反应;或CaCO3+2HCl=CaCl2+H2O+CO2↑;复分解反应.答案只要合理即可.)
(2)氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:O2或CO2;
(3)二氧化碳可以用浓硫酸干燥,干燥时要长进短出,故答案为:浓硫酸;a.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


对某些知识进行归纳,以对知识有更深刻的理解和认识.下列归纳和总结的关系,正确的是( )
| A. | 单质和化合物:交叉关系 | B. | 氧化反应和化合反应:并列关系 | ||
| C. | 化学肥料和复合肥料:并列关系 | D. | 酸性溶液和酸溶液:包含关系 |
 有关物质之间的部分转化关系如图所示,其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系,下列说法中正确的是( )
有关物质之间的部分转化关系如图所示,其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系,下列说法中正确的是( )| A. | 物质X是二氧化碳,它是一种常见的有机化合物 | |
| B. | 图中反应③可用于工业制取二氧化碳,该反应产生的生石灰用来做干燥剂 | |
| C. | 反应②一定是复分解反应 | |
| D. | 向Ca(OH)2溶液中加入CaO,所得溶液的溶质质量分数一定增大 |
| A. | 浓硫酸 | B. | 生石灰 | C. | 浓盐酸 | D. | 氢氧化钠 |
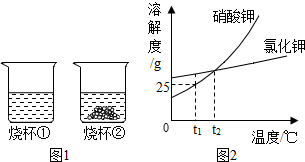 t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.
t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.



 如图为a、b两物质的溶解度曲线,据图回答:
如图为a、b两物质的溶解度曲线,据图回答: