题目内容
俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形.如图为元素周期表的部分元素的相关信息,利用下表回答相关问题
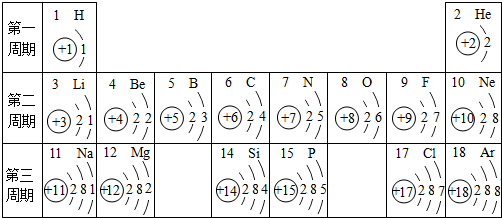
(1)请指出16号元素原子结构示意图中的最外层电子数 化学反应中该原子比较容易 (填“得到”或“失去”)电子变成离子;
(2)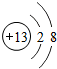 表示的是 (填离子符号);
表示的是 (填离子符号);
(3)如图中最活泼的金属元素与地壳中含量最多的元素组成的化合物是 (填化学式,任意填写一种);
(4)如图中第二、三周期元素最外层电子数的变化规律是 .

(1)请指出16号元素原子结构示意图中的最外层电子数
(2)
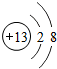 表示的是
表示的是(3)如图中最活泼的金属元素与地壳中含量最多的元素组成的化合物是
(4)如图中第二、三周期元素最外层电子数的变化规律是
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据原子结构示意图来分析其最外层电子数和得失电子的情况;
(2)根据粒子结构示意图分析;
(3)根据地壳中含量最多的元素是氧元素,该表中活泼的金属元素如:钠、镁、铝的化合价和化学式的书写方法书写化学式;
(4)根据表中各元素最外层电子数的特点分析规律.
(2)根据粒子结构示意图分析;
(3)根据地壳中含量最多的元素是氧元素,该表中活泼的金属元素如:钠、镁、铝的化合价和化学式的书写方法书写化学式;
(4)根据表中各元素最外层电子数的特点分析规律.
解答:解:(1)由16号元素也就是硫元素的原子结构示意图可知,其最外层电子数为6,在化学反应中易得电子;
(2)此粒子结构图中质子数为13,是铝元素,核外有10个电子,是阳离子,故符号为Al3+;
(3)在此表中,钠元素是最活泼的金属元素,通常在化合物中显+1价,氧-2价,所形成化合物的化学式为Na2O;
(4)观察表中第二、三周期各元素最外层电子数的变化可以看出最外层电子数从左到右由1递增到8.
故答案为:(1)6;得到;(2)Al3+;(3)Na2O;(4)从1--8逐渐递增.
(2)此粒子结构图中质子数为13,是铝元素,核外有10个电子,是阳离子,故符号为Al3+;
(3)在此表中,钠元素是最活泼的金属元素,通常在化合物中显+1价,氧-2价,所形成化合物的化学式为Na2O;
(4)观察表中第二、三周期各元素最外层电子数的变化可以看出最外层电子数从左到右由1递增到8.
故答案为:(1)6;得到;(2)Al3+;(3)Na2O;(4)从1--8逐渐递增.
点评:本题考查学生根据原子结构示意图分析总结元素周期律及对元素的性质与最外层电子数的关系的理解与掌握,并能在解题中灵活应用.

练习册系列答案
相关题目
钙是人体必须的一种常量元素.如图1是钙元素的一种粒子结构示意图.

(1)该粒子的符号为 .
(2)若该粒子核内的中子数为20,则其相对原子质量为 .
(3)如图2所示的微粒中,与钙原子的化学性质相似的是 .

(1)该粒子的符号为
(2)若该粒子核内的中子数为20,则其相对原子质量为
(3)如图2所示的微粒中,与钙原子的化学性质相似的是
能在pH为1的溶液中大量共存,且溶液为无色透明的一组物质是( )
| A、FeCl3、CuSO4、KCl |
| B、BaCl2、Na2SO4、NaOH |
| C、CaCl2、K2CO3、AgNO3 |
| D、K2SO4、KNO3、NH4NO3 |
 如图是学生经常使用的交通工具--自行车,请完成下列各题:
如图是学生经常使用的交通工具--自行车,请完成下列各题: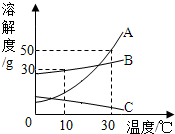 如图是A、B、C三种物质的溶解度曲线,根据如图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据如图回答下列问题: